药品不良反应数据库的作用是收集、记录和分析药品使用过程中可能出现的不良反应信息。这些数据库通常由医药监管机构、医药数据公司、医疗机构和科研机构等建立和维护,在监测和评估药品的安全性、发现和确认新的不良反应、支持药品监管决策、提供医学信息和警示等方面都起到至关重要的作用,有助于确保药物的安全性和有效性,减少患者的不良反应风险。
目前世界各地存在多个药品不良反应数据库,比较知名的如美国食品药品监督管理局(FDA)药品不良反应数据库、欧洲药品不良反应数据库(EudraVigilance)、英国国家药品不良反应数据库(Yellow Card Scheme)、澳大利亚药物不良反应数据库(Australian Adverse Drug Reactions Database)、加拿大药品不良反应数据库(Canada Vigilance)等,这些药品不良反应数据库因地区和国家差异数据各异,这也直接导致相关工作者想要去全面了解不良反应信息时需要比对多个国家数据非常不便。
为此部分医药数据公司开始了药品不良反应数据库的整合工作,如药融云医药数据库系统V4.0中的药品不良反应数据库就整合了全球各地多个国家的不良反应报告数据,总共收载数据超1500万多条,包含病例报告中的药物信息、主要可疑物、相互作用药物、不良事件、制造商、给药途径、剂量、适应症、报告类型、报告来源等信息。详细查询步骤如下:
①进入药融云官网--> 选择企业版--> 登录注册-->申请试用企业版-->选择‘药品研发’-->选择‘不良反应报告’数据库

②如点击上图结果展示区域中的‘Bortezomib’,可跳转查看到的详细信息如下

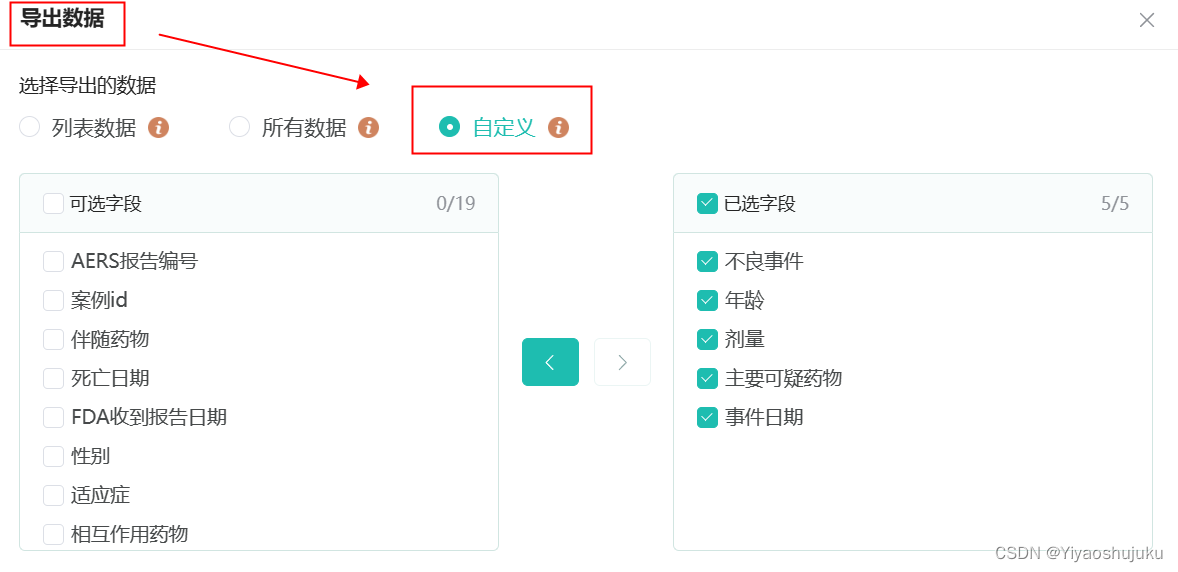
③点击‘导出’或下载图标,可看到下图页面,通过选择自定义下载,可随意筛选想要下载的目标字段
一键检索、条件检索、高级检索以及多维度条件筛选等功能为用户提供了更多的自定义选项,使他们能够从庞大的数据中筛选出所需的信息,并展开多维度的分析。例如,通过选择报告类型为加速报告,用户可以了解新出现的或严重的药物不良反应情况。选择医生、药剂师及其他卫生专家作为报告者职业,可以增加报告的可信度和专业度。而根据患者的年龄、性别等分组,可以探索药物不良反应在不同性别、年龄组之间是否存在差异,找出高危人群,并提出相应的安全警示,以避免潜在风险。这些功能的引入使得药物不良反应数据库的使用更加灵活和个性化,为用户提供了更准确、全面的信息,并支持深入的数据分析和决策。





![[SQLITE_ERROR] SQL error or missing database (near “=“: syntax error)【已解决】](https://img-blog.csdnimg.cn/efa74a403eb34398894eece1b6868560.png)