什么是CAR-T?
CAR-T是Chimeric Antigen Receptor T-cell(嵌合抗原受体T细胞)的缩写。它是通过将人体自身的T细胞进行基因改造,使其具有针对肿瘤细胞的抗原特异性,从而增强免疫系统对肿瘤细胞的攻击能力。CAR-T治疗的过程,其大致分为以下几个步骤:
- T细胞采集:从患者的血液中提取T细胞;
- 基因改造:将基因工程技术应用于T细胞,将其转导为携带CAR(嵌合抗原受体)的细胞;
- 体外扩增:将改造后的CAR-T细胞进行体外扩增,使其数量增多;
- 治疗注射:将大量的CAR-T细胞重新注射到患者体内;
- 杀伤肿瘤:CAR-T细胞识别和结合肿瘤细胞表面的特定抗原,释放细胞毒素,杀死肿瘤细胞。
- 持续观察:对患者进行密切观察,监测治疗效果和可能的副作用。

CAR-T免疫治疗流程
CAR的分子设计
在分子水平上,CAR-T细胞杀伤肿瘤细胞是基于
- CAR分子的胞外抗原结合域特异性识别肿瘤抗原;
- 识别信号传导至CAR分子的胞内结构域;
- 胞内结构域活化T细胞,使细胞增殖、合成穿孔素和颗粒酶、释放细胞因子等,杀伤肿瘤细胞。
因此,为了最大程度地发挥其功能,CAR分子的结构设计是至关重要的。
CAR分子由4个主要成分构成:
- 细胞外抗原结合结构域:赋予CAR分子靶点特异性的功能。它的原理是将抗体的可变重链(VH)和可变轻链(VL)连接形成单链可变区段(scFv),用以特异性识别肿瘤表面抗原。
- 铰链区:连接跨膜域和细胞外单元的结构区。铰链的作用是提供空间灵活性,可以克服空间位阻,并且拥有合适的长度允许抗原结合域接近目标表位。
- 跨膜结构域:主要功能是将CAR分子锚定在T细胞的细胞膜上。有研究表明,跨膜区可能影响CAR分子的表达水平、稳定性,在信号传导中发挥作用。
- 细胞内信号传导结构域:CAR分子共刺激的效果是CAR工程中备受关注的焦点。1-3代CAR分子的主要区别来自于胞内的共刺激结构域。两种最常见的、经由FDA批准的共刺激域CD28和4-1BB都具有高效的活化T细胞的效果,可诱导T细胞执行不同的功能。

CAR分子设计蓝图
CAR-T细胞疗法的局限性和实体瘤治疗中面临的挑战
CAR-T细胞疗法的局限性,主要包括威胁生命的细胞因子风暴(CRS)、神经毒性、 抗原逃逸、治疗效果的持久性等。特别对于实体瘤的治疗,由于肿瘤微环境等因素的影响,目前在临床上还未取得突破性成功。

CAR-T细胞疗法的局限性包括:A. 抗原逃逸;B. 脱靶效应;C. CAR-T细胞转运及浸润;D. 免疫抑制微环境;E. CAR-T细胞相关的毒性。
CAR-T细胞治疗是一种在近十年中新兴的免疫疗法,过去主要用于治疗血液肿瘤,并取得了巨大成功,但随后在对实体瘤的治疗中却遇到了很多难题。主要包括肿瘤抗原异质性和细胞的回输和对肿瘤组织的浸润
(1)肿瘤抗原异质性
肿瘤抗原异质性是CAR-T细胞疗法对抗实体瘤的障碍之一。肿瘤抗原主要分为两种:肿瘤相关抗原(TAA)和肿瘤特异性抗原(TSA):TAA在肿瘤细胞中高表达,在正常组织细胞中也有表达,但表达量较低;TSA仅在肿瘤细胞中表达,不在正常组织细胞中表达,因此也是最理想的抗原靶点。由于TSA的发现和筛选极为困难,CAR分子最常用的识别靶点是TAA,因此不同类型肿瘤细胞对于TAA的多样性表达可能会影响CAR-T细胞对癌细胞的识别,并降低CAR-T治疗的效果。
目前已经有多种方法使CAR-T细胞靶向识别多种肿瘤相关抗原,例如在单一的T细胞上共表达多种CAR分子、可编程式的CAR表达调控等。表达两个或多个抗原识别结构域,可以使单个CAR-T细胞识别肿瘤细胞上表达的多个抗原,从而消除抗原异质性带来的不利影响。

实体瘤中的免疫抑制微环境:a. 效应细胞和靶细胞;b. 免疫抑制细胞和细胞因子;c. 物理屏障;d. 肿瘤内部微环境;e. 其他免疫抑制因素
(2)CAR-T细胞的回输和对肿瘤组织的浸润
CAR-T细胞可以存在于血液和淋巴系统中,因此对于血液瘤,CAR-T细胞具有更多的机会和血液肿瘤细胞接触,而在实体瘤中,CAR-T细胞较难通过血液系统穿透肿瘤组织。此外,由于缺乏参与T细胞渗透到肿瘤组织中的趋化因子表达,以及实体瘤中存在致密的纤维化基质,导致CAR-T细胞迁移和侵入肿瘤细胞的能力降低。
在很多报道中已有将CAR-T细胞直接局部注入到肿瘤位点(Tumor site)中的方法,比如脑部、乳腺、胸膜、肝脏等。CAR-T细胞的局部注射也可能降低脱靶效应带来的风险。然而,许多实体瘤具有转移性,是局部注射CAR-T细胞的一大难点。另一方面,一些临床研究中使用趋化因子介导CAR-T细胞的运输,增强对肿瘤的定位。例如巨噬细胞集落刺激因子1受体 (CSF-1R) 在CAR-T 细胞中的表达使这些细胞对CSF-1(一种在许多实体瘤中富集的单核细胞趋化因子)产生反应,在增强CAR-T细胞增殖信号传导的同时,不影响细胞的杀伤毒性。
实体瘤的肿瘤微环境在促进肿瘤生长和增殖的同时,对CAR-T细胞造成了免疫抑制。包括免疫抑制细胞如调节性T细胞(Treg)、髓源抑制细胞(MDSC)、肿瘤相关巨噬细胞(TAM),实体瘤中产生的生长因子、局部细胞因子,CTLA-4和PD-1等免疫检查点分子等,这些复合环境下的肿瘤微环境会极大地限制CAR-T细胞的疗效。
CAR-T突破实体瘤的研究最近出现的新进展
近几年,随着科学家对CAR-T治疗的研究不断深入,科研工作者近些年已经通过各种改造升级手段,在对多种实体瘤的治疗中也取得了新的进展。
1. 通过嵌合正交细胞因子受体增强CAR-T治疗实体瘤效果
近两年出现了很多改造CAR-T治疗实体瘤的研究,其中最值得深入了解的就是在2022年由斯坦福大学的Christopher Garcia,宾夕法尼亚大学的Carl H. June以及加州大学洛杉矶分校的Antoni Ribas、Anusha Kalbasi等,在国际著名杂志《Nature》上发表的题为:Potentiating adoptive cell therapy using synthetic IL-9 receptors 的研究论文。其实早在2018年,同样是Christopher Garcia作为通讯作者,就已经在Science发表论文,当时就已经提出了基于正交细胞因子及其受体的理念来改造CAR-T。
正交细胞因子受体是正常受体的一种突变形式,可选择性地结合突变的细胞因子,而不与正常的细胞因子结合。在这项研究中,作者首先将正交小鼠IL-2受体o2R的ICD替换为γc(receptors for common γ-chain)细胞因子IL-4,IL-7,IL-9和IL-21受体的ICD,创建嵌合正交受体。并选择oIL-2克隆3A10作为受体配体。分析筛选发现通过o9R的信号转导导致STAT1,STAT3,STAT5有效磷酸化。这种效果与野生型IL-9受体已知信号传导一致。随后进一步分析发现o9R信号转导是剂量依赖的,并且对MSA-oIL2具有特异性,并且o2R或者o9R的表达不影响野生型IL-2诱导的STAT信号传导。

嵌合正交 IL-2 受体揭示了 T 细胞中 IL-9R 信号传导的特性
紧接着通过实验,作者发现在这些γc细胞因子中,IL-9更值得研究——与其他γc 细胞因子不同,IL-9 信号在自然发生的 T 细胞中并不活跃。因此,人工合成的嵌合正交 IL-9 受体(o9R)将使过继性 T 细胞在对抗肿瘤时更加强大。进一步研究发现,通过o9R发出信号的 T 细胞以伴随激活STAT1、STAT3和STAT5 而区分,并呈现出一种独特的干细胞和杀伤细胞的混合特性。与之前的o2R T细胞相比,o9R T细胞在两种难治性的黑色素瘤和胰腺癌小鼠实体瘤模型中具有更好的抗肿瘤效果,最高治愈率超过50%!
作者接下来开始研究o9R在实体瘤过继细胞疗法中的体内信号转导,他们使用转基因pmel小鼠的T细胞,它表达内源性特异性gp100的T细胞受体,gp100是黑色素细胞抗原。在B16中过表达。研究发现pmel T细胞中o2R和o9R的STAT信号和细胞增殖可以反映野生型小鼠的o2R和o9R T细胞的状况。评估发现在没有淋巴清除的情况下,o9R pmel T细胞在该模型中可以延长小鼠生存期,实现较好的抗肿瘤作用。尽管o9R信号的增殖作用较弱,但是o9R可以改善肿瘤中T细胞浸润,IFN-γ表达增加,o9R pmel T细胞体外溶细胞能力更高。作者通过RNA-seq也证实了这些表型。而且除却与干细胞样记忆T细胞的相关变化,作者还观察到与T细胞经典激活表型相关基因富集。这表明这群细胞具有混合表型。

o9R 信号赋予 pmel T 细胞在没有淋巴细胞耗竭的情况下具有抗肿瘤功效。
最后,作者用免疫治疗抵抗的表达间皮素的胰腺癌模型中构建CAR为基础的过继治疗模型。用腺病毒载体编码oIL2(Ad-oIL-2) 加 CAR-o2R 联合治疗 CAR-o9R 导致 12 只小鼠中有 8 只(67%)完全消退,并且未观察到细胞因子释放综合征或者肿瘤溶解综合征。最后,作者证实了无论是将细胞因子对小鼠进行全身性递送,还是直接注射到肿瘤中,这种疗法都是有效的。在各种情况下,用人工合成的正交 IL-9 受体改造的 T 细胞都表现得更优秀,能够治愈了一些难治性实体肿瘤。
总的来说,这项研究表明,通过人工合成的正交 IL-9 及其受体 IL-9R,可以无需化疗或放疗清除免疫系统的情况下激活CAR-T细胞,使之获得了新的功能,增强对难治性实体肿瘤的抗肿瘤活性,这些发现将为人类治疗实体瘤打开了一扇新的大门。
2. 肿瘤特异性受体信号协助CAR-T进入冷肿瘤
去年另一项有关改造CAR-T的重磅研究,是加利福尼亚大学旧金山分校Wendell A. Lim教授课题组在《Science》杂志上,发表的题为“Synthetic cytokine circuits that drive T cells into immune-excluded tumors”的论文。该研究专门针对嵌合抗原受体(CAR)T细胞,在对具有免疫抑制微环境的实体瘤(冷肿瘤)治疗无效的问题,作者设计了肿瘤特异性synNotch受体局部诱导细胞因子IL-2产生的信号回路。
这些信号回路有效地增强CAR T细胞浸润和清除免疫排斥型肿瘤,并且没有全身毒性。最有效的IL-2诱导回路绕过抑制机制以自分泌和T细胞受体(TCR),或CAR独立的方式起作用。这些工程细胞在靶肿瘤中建立了立足点,合成Notch诱导的IL-2产生能够启动CAR介导的T细胞扩增和细胞杀伤。因此,有可能重建合成T细胞回路,以激活抗肿瘤反应最终所需的输出,但其方式避开了肿瘤抑制的关键点。

合成的 synNotch→IL-2 电路可以独立于 TCR 激活或与 T 细胞杀伤协同驱动局部 T 细胞增殖。
随后,研究者给synNotch-IL-2环路T细胞设计一种新型的AND门,治疗性T细胞在触发其充分的细胞毒性反应之前需要识别两个抗原:T细胞活化所需的TCR抗原和诱导IL-2产生所需的synNotch抗原。在这种情况下,作者使用了anti GFP-synNotch→sIL-2合成细胞因子回路。通过要求TCR抗原(NYESO-1)和synNotch抗原同时存在。当同时表达anti-NY-ESO-1 TCR和anti-GFP synNotch→sIL-2环路的T细胞治疗小鼠时,双靶向的NY-ESO+/GFP+肿瘤体积显著减小。
为了研究在完全免疫正常的小鼠肿瘤模型中局部IL-2产生的影响,研究者在原代小鼠T细胞中构建了anti-mesothelin CAR与synNotch-IL-2环路同时表达。随后作者发现,改造后CAR-T细胞介导的杀伤作用使得肿瘤消退。

自分泌合成 IL-2 回路可显着提高 T 细胞对多种免疫排除同基因肿瘤模型的细胞毒性。
细胞递送的IL-2是与治疗性T细胞协同作用的有力工具,细胞因子如IL-2长期以来被认为是抗肿瘤免疫的强大刺激因子。然而,众所周知,全身性IL-2递送具有高度毒性,导致广泛的副作用,从而大大限制了其治疗用途。作者利用工程化细胞的能力来识别肿瘤,并在需要的地方准确地局部递送IL-2。细胞介导的局部细胞因子(IL-2)递送可以有效地克服免疫抑制,增强CAR-T细胞,以有效地清除多种免疫排斥肿瘤模型(胰腺癌和黑色素瘤)。
机体产生细胞因子的不同方式,对其成功发挥相应功能是至关重要的。首先,细胞因子的产生必须是动态调节的(可诱导的),但IL-2的持续产生可能加剧脱靶毒性。其次,要绕过肿瘤微环境对TCR/CAR的抑制,IL-2产生的诱导必须独立于TCR激活途径。作者通过研究发现,这一约束的一个有力解决方案是设计一种合成信号转导途径,该途径是肿瘤触发的,但绕过天然CAR/TCR激活途径。使用检测肿瘤的synNotch受体来驱动IL-2的产生,为实现这一目标提供了一种简单而模块化的方法。
3. 打造干细胞样CAR-T发挥持久抗肿瘤作用
2023年,两篇最近发表的改造CAR-T细胞的研究成果,均在不同实体瘤上达到更好的治疗效果。其中一项研究是澳大利亚Peter MacCallum癌症中心的研究人员在《Science Translational Medicine》杂志上发表的题为:“TSTEM-like CAR-T cells exhibit improved persistence and tumor control compared with conventional CAR-T cells in preclinical models” 的研究成果。
虽然目前FDA已批准了5款CAR-T细胞疗法上市,用于治疗白血病、淋巴瘤和骨髓瘤等血液瘤,但在更主要的癌症类型实体瘤中,CAR-T细胞疗法效果有限。这与CAR-T细胞扩增不良、持久性不佳以及T细胞耗竭等多种因素有关。为了解决这一难题,作者开发了一种基于干细胞样T细胞(TSTEM)的新型CAR-T细胞疗法,相较于基于传统T细胞的CAR-T细胞,TSTEM CAR-T细胞扩增能力更强, 并在临床前研究中证明其对实体瘤有效。同时,这也是CAR-T细胞疗法在实体瘤治疗中的重要突破。
 早期表型 CAR-T 细胞表现出 TSTEM 样表型,缺乏免疫检查点分子表达。
早期表型 CAR-T 细胞表现出 TSTEM 样表型,缺乏免疫检查点分子表达。
相较于传统CAR-T治疗,在接受记忆T细胞富集的CAR-T细胞治疗的癌症患者,由于CAR-T细胞的扩增和持久性,可以表现出更好的癌症控制效果。人记忆T细胞包括干细胞样CD8+ 记忆T细胞祖细胞,可以成为功能性的干细胞样T细胞(TSTEM) 或功能障碍的耗竭前体T细胞(T-PEX)。研究团队在一项CAR-T细胞治疗1期临床试验(NCT03851146)中证明,干细胞样T细胞(TSTEM)在输注的CAR-T细胞中含量较低,输注的CAR-T细胞在患者体内表现出较差的持久性。
为了解决这一问题,研究团队开发了一种生产方案,以快速生成干细胞样T细胞(TSTEM),可在短短6天内生成功能完善的TSTEM CAR-T细胞,而不是标准的14天,这为未来更经济、高效的CAR-T细胞治疗打开了大门。与传统CAR-T相比,T-STEM CAR-T细胞增殖能力更强,细胞因子分泌也有所增加。这些反应依赖于在TSTEM CAR-T细胞生成过程中CD4+ T细胞的存在。随后,作者在多个临床前动物模型中,过继移植TSTEM CAR-T细胞可以更好地控制小鼠肿瘤生长,以及抵抗肿瘤复发。这些更有利的结果与TSTEM CAR-T细胞持久性的增加和记忆T细胞库的增加有关。

TSTEM-like CAR-T 细胞在体内表现出增强的持久性和肿瘤控制。
总之,在这项研究中作者描述了一种易于复制的方案,以产生具有增强增殖和自我更新能力的人类干细胞样CAR-T细胞。这些干细胞样CAR-T细胞也可以在肿瘤部位形成效应CAR-T细胞,通过抗pd-1辅助治疗可以增强这种效应。许多临床试验正在研究CAR-T疗法在实体肿瘤中的应用,然而迄今为止报道的临床反应有限。患者反应不理想的关键机制包括体内有限的CAR-T细胞持久性。在这里,作者开发了一种新型的CAR-T细胞,具有强大的增殖潜力,能够提高在体内存在的持久性。因此,作者提出的这种CAR-T改造方案具有直接和广泛的意义,同时具有结合干细胞样CAR-T细胞的未来试验方案的潜力,特别是与免疫检查点阻断联合,可用于更有效的治疗实体瘤。
4. γδ CAR-T在骨转移癌症中表现优异
上述的所有研究都是集中在传统的αβT细胞上,而最近发表在《Science Advances》杂志上的另一项篇名为:“γδ-Enriched CAR-T cell therapy for bone metastatic castrate-resistant prostate cancer”的文章,则是通过改造另一种固有免疫样γδCAR-T细胞来实现更好的抗实体瘤的效果。我们常说的T 细胞其实是指αβT细胞,约占 T 细胞总量的65%-70%,其表面的 T 细胞受体(TCRs)由两条糖蛋白链组成α 链和β链。而γδ T细胞是 T细胞的一个亚群,占所有 T 淋巴细胞的0.5%-5%,其 TCRs 由 γ链和 δ 链组成,主要存在于上皮和粘膜组织,比如皮肤、肠道等。虽然含量不多,但γδ T细胞没有抗原特异性,因此具有更广泛的肿瘤杀伤作用。
在这项研究中,作者采用了一种使用γδ的嵌合抗原受体(CAR)-T细胞和唑来膦酸盐 (ZOL)治疗骨转移性前列腺癌(mCRPC)的组合策略。在骨mCRPC的临床前小鼠模型中,靶向前列腺干细胞抗原 (PSCA) 的γδCAR-T细胞诱导肿瘤快速显着消退,同时增加存活率并减少癌症相关骨病。最终该研究的数据表明,内源性 Vγ9Vδ2 T 细胞受体的活性在CAR-T 细胞中得以保留,从而允许对肿瘤细胞进行双受体识别。

CAR 内域设计的影响。
为了产生γδCAR-T细胞,研究人员首先用第二代CD28共刺激CAR构建体(28t28Z) 转导富含Vγ9Vδ2 的T细胞,当转导至αβT细胞时,该构建体先前已显示出对表达PSCA 的肿瘤的抗肿瘤功效。然而,修饰的CAR 的γδT 细胞表达显然更胜一筹,其中CD28衍生的铰链和跨膜结构域(但没有信号部分)被 CD8α衍生的铰链/跨膜(8t28Z)取代。表达这些CAR 的γδT细胞表现出白细胞介素2受体 (IL-2Rβ) 的β亚基的更高表达,这些结果表明,结构元素的轻微修改可以大大增强CAR表达。而表达CD28共刺激的第二代CAR 的γδT细胞显示出最大的IFN-γ(IFN-γ分泌可以调节实体瘤的肿瘤微环境并增加 CAR-T 细胞的功效)分泌和靶向前列腺癌细胞的细胞毒性。
接下来,他们将实验转移到小鼠模型上,结果表明CAR-T细胞显着减小了肿瘤的大小并提高了存活率,而且毒性有限。为了评估抗PSCA 的γδCAR-T细胞在体内抗肿瘤活性,研究者将表达PSCA的C4-2B前列腺癌细胞(每次注射2.0×105个)接种到6 周龄小鼠的左右胫骨中雄性NSG (NOD.Cg-Prkdcscid Il2rgtm1Wjl/SzJ) 小鼠 (n=10),并通过生物发光成像监测作为肿瘤负荷的读数。
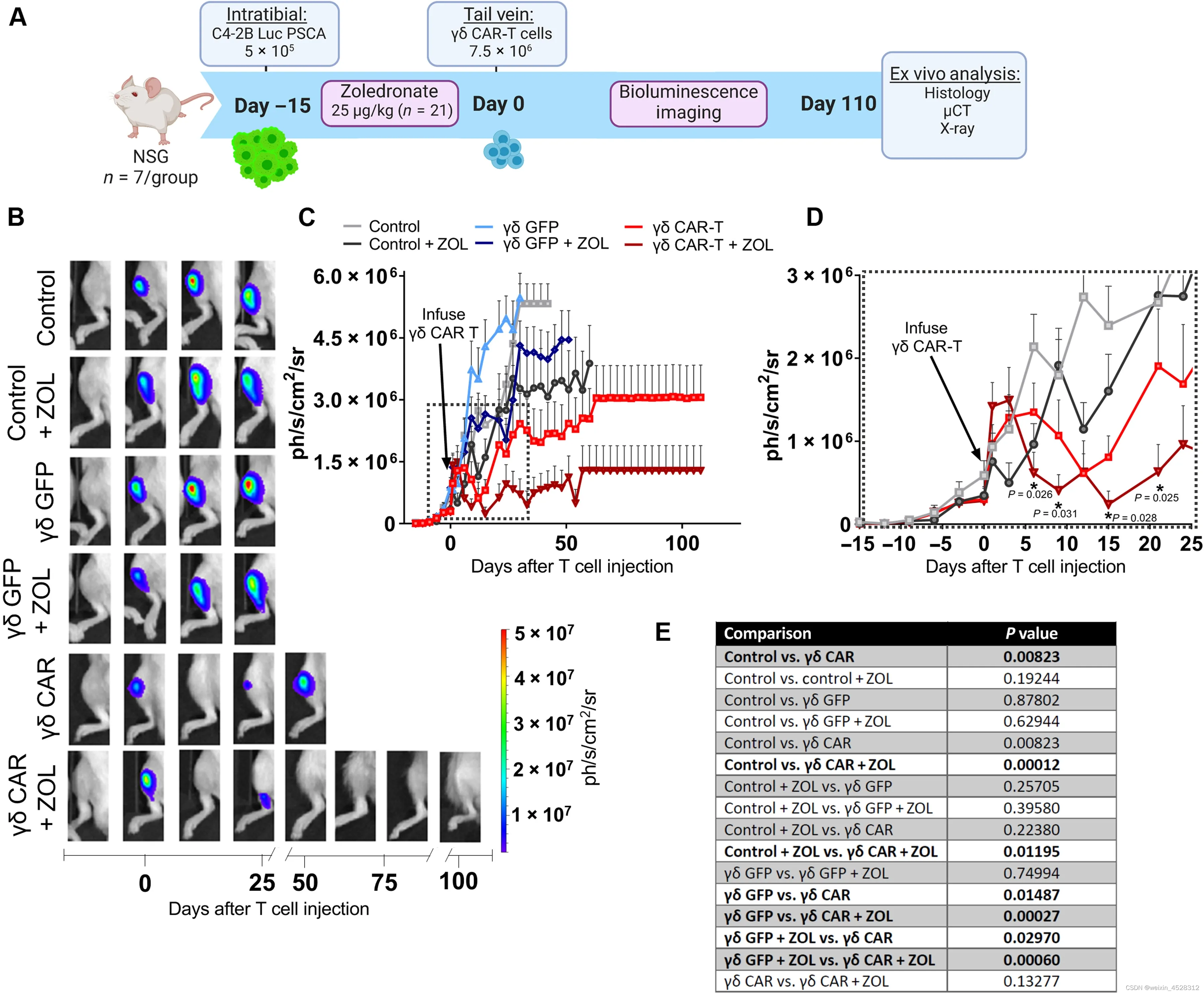
ZOL 增强富含 γδ 的 CAR-T 细胞介导的胫骨内前列腺肿瘤消退。
10天后,根据检测到的不同光信号将小鼠随机分为两组,一组作为未处理的对照组,另一组通过尾静脉接种接受抗PSCA γδCAR-T 细胞 (1.5×107)。随后的生物发光成像显示,用抗 PSCA γδ CAR-T疗法治疗的小鼠表现出快速且显着的肿瘤消退(P=0.009),在 T 细胞转移后的24小时内持续长达30天。在稍后的时间点,五只经抗PSCA γδCAR-T 治疗的小鼠中有两只出现复发,但随即观察到这些肿瘤的生长与未治疗的对照肿瘤相比显然要慢得多。
总而言之,这一研究是第一次评估γδT细胞表达CAR和治疗骨转移性前列腺癌。具有迅速达成临床转化的潜力,猜测用不了多久就会有类似的一款CAR-T申报mCRPC的临床。
小结
无论是通过嵌合正交细胞因子受体,肿瘤特异性synNotch受体,还是生产干细胞样T细胞的CAR-T细胞,这些针对传统αβT细胞的改造方式;还是通过直接改造γδT细胞(没有MHC分子限制),以提高其普适性;我们都可以看到近些年在针对实体瘤的CAR-T改造中取得了不错的成果。可以说,这些研究成果都在不同角度上给我们提供了促进CAR-T杀伤肿瘤细胞的思路。
但除此之外,未来CAR-T发展方向还仍然主要从以下这些方面着手:
1.扩大适应症范围:目前CAR-T细胞疗法主要用于治疗血液系统肿瘤,如急性淋巴细胞白血病和非霍奇金淋巴瘤。虽然目前已经在动物模型中取得初步不错的效果,或者在一部分黑色素瘤也有较好的疗效,但未来CAR-T发展的首要任务仍然需要扩大适应症范围,将CAR-T细胞疗法应用于更多类型的实体肿瘤,如肺癌、乳腺癌、结直肠癌等。研究人员将努力寻找更多的肿瘤抗原,并开发具有更广泛抗原特异性的CAR-T细胞。
2.提高治疗效果:CAR-T细胞疗法在某些患者中取得了显著的临床疗效,但仍有患者出现复发或无效的情况。未来的发展趋势将集中在提高CAR-T细胞的治疗效果和持久性。这可能包括改进CAR-T细胞的设计,以增强其肿瘤识别和杀伤能力,以及开发联合治疗策略,如与其他免疫疗法、放疗或化疗的联合应用。
3.减轻副作用:CAR-T细胞治疗可能引发一系列副作用,包括细胞因子释放综合征(CRS)和CAR-T细胞相关性脑病(CRES)。未来的发展趋势将集中在减轻副作用并提高治疗的安全性。研究人员将寻找更好的管理和预防副作用的方法,并改进CAR-T细胞的构建和调控策略,以减少不必要的激活和副作用。随着精准医疗的发展,CAR-T细胞治疗也将朝向个体化治疗方向发展。通过基因检测和肿瘤特征分析,可以选择最适合患者的CAR-T细胞治疗策略。这可能包括选择特定的CAR-T细胞构建、剂量和治疗方案,以提高治疗的针对性和效果。
4.生产和可及性改进:CAR-T细胞治疗的生产过程复杂且昂贵,限制了其广泛应用的可能性。未来的发展趋势将包括改进生产工艺和降低成本,以提高CAR-T细胞治疗的可及性和可持续性。新的生产技术和自动化系统的引入可能会加速CAR-T细胞的生产和供应,只有将成本降下来才会使得CAR-T可以为更广大的肿瘤患者带来实质的帮助,要不然都是纸上谈兵。
总而言之,CAR-T疗法攻克实体瘤治疗中的局限,可以说是目前该领域面临的最紧迫的挑战之一。事实上,全球约90%的癌症病例是实体肿瘤,未满足的临床需求仍十分巨大。但一直以来,与血液肿瘤相比,实体瘤上缺乏选择性和高表达的表面抗原,抗原异质性,免疫抑制性微环境,以及实体瘤厚实的物理屏障等因素,使得经静脉注射的CAR-T细胞不仅难以进入肿瘤并以战胜癌症所需的数量与肿瘤结合,也难以在肿瘤病灶形成的不利微环境中生存,并有效发挥作用。
目前,CAR-T细胞治疗作为一种创新的肿瘤治疗方法,在全球科研工作者的共同努力下,取得了令人鼓舞的进展。它不仅在血液系统肿瘤的治疗中取得了显著的成功,并在实体肿瘤领域也显示出巨大的潜力。然而,CAR-T细胞治疗仍面临着一些挑战,包括浸润到实体瘤中以增加治疗效果、批量生产的成本和复杂性、副作用的管理等。随着技术的进步和临床经验的积累,预计CAR-T细胞治疗将逐渐得到改进和优化,可以为更多实体肿瘤患者带来益处,并成为未来肿瘤治疗领域的重要方式之一。
[参考文献]
[1] Sterner, R. C., & Sterner, R. M. (2021). CAR-T cell therapy: current limitations and potential strategies. Blood Cancer Journal, 11(4), 1-11.
[2] Bridgeman, J. S., Hawkins, R. E., Bagley, S., Blaylock, M., Holland, M., & Gilham, D. E. (2010). The optimal antigen response of chimeric antigen receptors harboring the CD3ζ transmembrane domain is dependent upon incorporation of the receptor into the endogenous TCR/CD3 complex. The Journal of Immunology, 184(12), 6938-6949.
[3] Guedan, S., Posey Jr, A. D., Shaw, C., Wing, A., Da, T., Patel, P. R., ... & June, C. H. (2018). Enhancing CAR T cell persistence through ICOS and 4-1BB costimulation. JCI insight, 3(1).
[4] Kalbasi A, Siurala M, Su LL, Tariveranmoshabad M, Picton LK, Ravikumar P, Li P, Lin JX, Escuin-Ordinas H, Da T, Kremer SV, Sun AL, Castelli S, Agarwal S, Scholler J, Song D, Rommel PC, Radaelli E, Young RM, Leonard WJ, Ribas A, June CH, Garcia KC. Potentiating adoptive cell therapy using synthetic IL-9 receptors. Nature. 2022 Jul;607(7918):360-365.
[5] Kalbasi A, Siurala M, Su LL, Tariveranmoshabad M, Picton LK, Ravikumar P, Li P, Lin JX, Escuin-Ordinas H, Da T, Kremer SV, Sun AL, Castelli S, Agarwal S, Scholler J, Song D, Rommel PC, Radaelli E, Young RM, Leonard WJ, Ribas A, June CH, Garcia KC. Potentiating adoptive cell therapy using synthetic IL-9 receptors. Nature. 2022 Jul;607(7918):360-365.
[6] Meyran D, Zhu JJ, Butler J, Tantalo D, MacDonald S, Nguyen TN, Wang M, Thio N, D'Souza C, Qin VM, Slaney C, Harrison A, Sek K, Petrone P, Thia K, Giuffrida L, Scott AM, Terry RL, Tran B, Desai J, Prince HM, Harrison SJ, Beavis PA, Kershaw MH, Solomon B, Ekert PG, Trapani JA, Darcy PK, Neeson PJ. TSTEM-like CAR-T cells exhibit improved persistence and tumor control compared with conventional CAR-T cells in preclinical models. Sci Transl Med. 2023 Apr 5;15(690):eabk1900.
[7] Frieling JS, Tordesillas L, Bustos XE, Ramello MC, Bishop RT, Cianne JE, Snedal SA, Li T, Lo CH, de la Iglesia J, Roselli E, Benzaïd I, Wang X, Kim Y, Lynch CC, Abate-Daga D. γδ-Enriched CAR-T cell therapy for bone metastatic castrate-resistant prostate cancer. Sci Adv. 2023 May 3;9(18):eadf0108.