文章目录
- Radiomics-enhanced Deep Multi-task Learning for Outcome Prediction in Head and Neck Cancer
- 摘要
- 本文方法
- 实验结果
- Predicting Regions of Local Recurrence in Glioblastomas Using Voxel-Based Radiomic Features of Multiparametric Postoperative MRI
- 摘要
- 方法
- 实验结果
Radiomics-enhanced Deep Multi-task Learning for Outcome Prediction in Head and Neck Cancer
摘要
预后预测对头颈癌患者至关重要,因为它可以为早期治疗计划提供预后信息。放射组学方法已广泛应用于医学图像的预后预测。
然而,这些方法的局限性在于它们依赖于难以处理的肿瘤区域的人工分割。最近,人们提出了深度学习方法来进行端到端结果预测,以消除对人工分割的依赖。不幸的是,如果没有分割掩模,这些方法将把整个图像作为输入,这使得它们难以关注肿瘤区域,并且可能无法充分利用肿瘤区域内的预后信息。在这项研究中,我们提出了一个放射组学增强的深度多任务框架,用于头颈部肿瘤分割和结果预测挑战(HECKTOR 2022)的PET/CT图像结果预测。在我们的框架中,我们的新颖之处在于将放射组学作为我们最近提出的深度多任务生存模型(DeepMTS)的增强。DeepMTS共同学习预测患者的生存风险评分和肿瘤区域的分割掩码。从预测的肿瘤区域提取放射组学特征,并结合预测的生存风险评分进行最终预后预测,进一步利用肿瘤区域的预后信息。我们的方法在测试集上实现了0.681的c指数,在排行榜上排名第二,c指数仅比第一名低0.00068。
本文方法
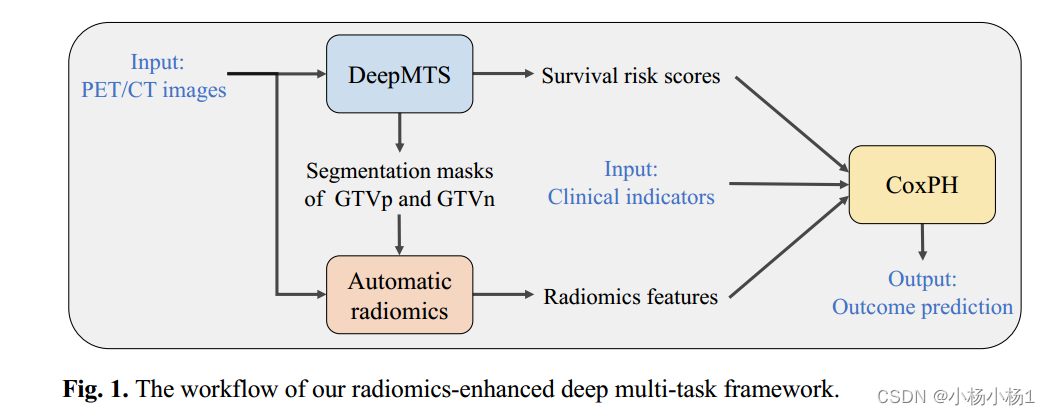
模型结构
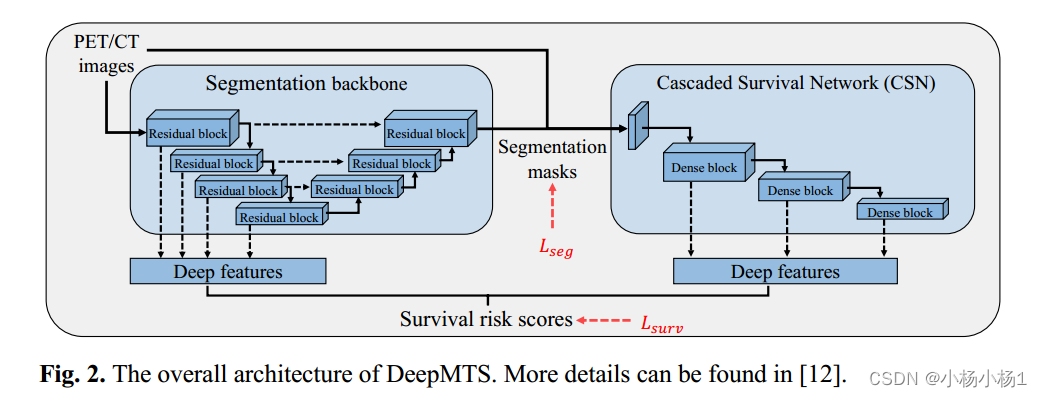
通过Pyradiomics从PET/CT图像的预测肿瘤区域中提取手工特征。预测的GTVp和GTVn掩码合并为单个掩码(GTVp和GTVn为1,否则为0)用于特征提取。提取的手工特征包括一阶统计量(FOS)、相邻灰调差矩阵(NGTDM)、灰阶运行长度矩阵(GLRLM)、灰阶大小区域矩阵(GLSZM)、灰阶协同矩阵(GLCM)和基于三维形状的特征。除了原始的PET/CT外,还使用了PET/CT的8个小波分解,得到了1689个放射组学特征。所有放射组学特征使用Z-score归一化进行标准化,然后通过最小绝对收缩和选择算子(LASSO)回归减少到7个判别放射组学特征。
我们在测试集上的结果是通过5倍交叉验证构建的5个模型的集合获得的。对于结果预测,首先对五个模型的检验结果进行Z-score归一化标准化,然后共同平均,得到最终的检验结果。对于肿瘤分割,我们尝试了两种集成方法:(i)首先对五个模型的测试结果进行平均,然后在0.5处设置阈值,得到最终的测试结果;(ii)首先对五个模型的测试结果在0.5处设置阈值,通过多数投票得到最终的测试结果。
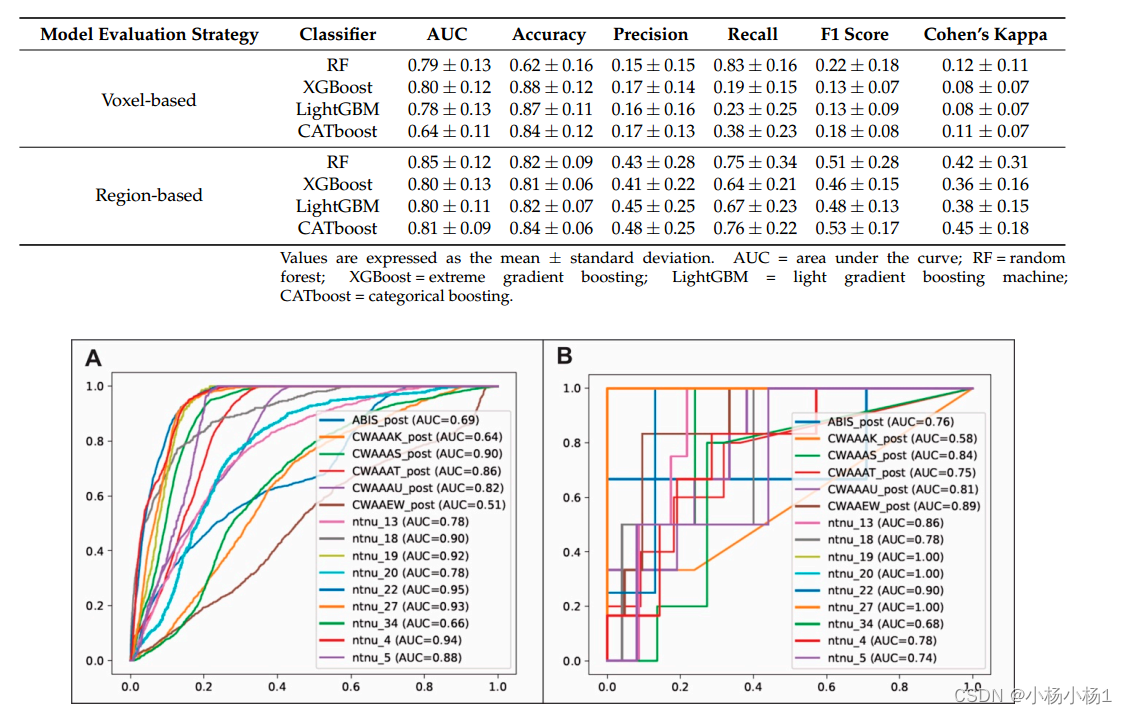
实验结果
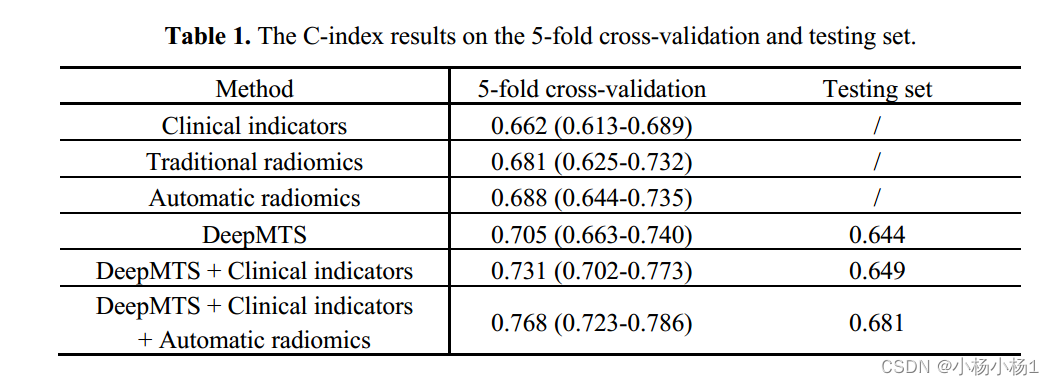
Predicting Regions of Local Recurrence in Glioblastomas Using Voxel-Based Radiomic Features of Multiparametric Postoperative MRI
摘要
全球接受的胶质母细胞瘤手术策略是切除增强肿瘤。
然而,肿瘤周围的浸润区会导致未来的肿瘤复发。
本研究旨在评估一种预测模型,该模型使用基于体素的磁共振成像(MRI)数据放射组学分析来识别未来复发的区域。这项多机构研究包括对诊断为胶质母细胞瘤的患者进行回顾性分析,这些患者接受了手术并完全切除了增强肿瘤。55例患者符合入选标准。研究样本分为训练(N = 40)和测试(N = 15)数据集。随访MRI用于基础真值定义,术后结构多参数MRI用于提取基于体素的放射学特征。采用可变形共配准对每位患者的MRI序列进行配准,随后在术后扫描中对肿瘤周围区域进行分割,并在后续扫描中对增强肿瘤进行分割。与增强肿瘤体素重叠的肿瘤周围体素被标记为复发,而不重叠的体素被标记为不复发。从肿瘤周围区域提取基于体素的放射学特征。训练四个基于机器学习的分类器进行递归预测。采用基于区域的评价方法对模型进行评价。分类提升(CatBoost)分类器获得了最好的性能
方法
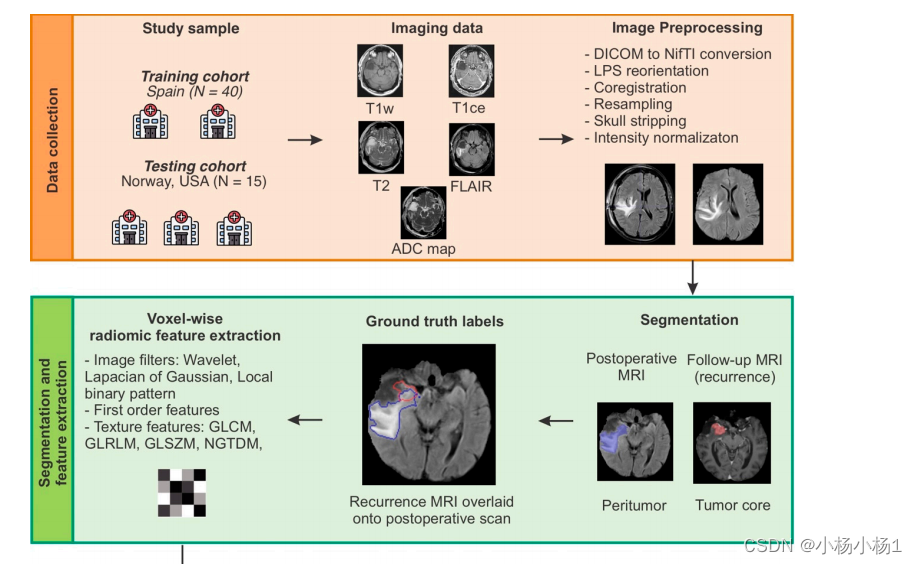
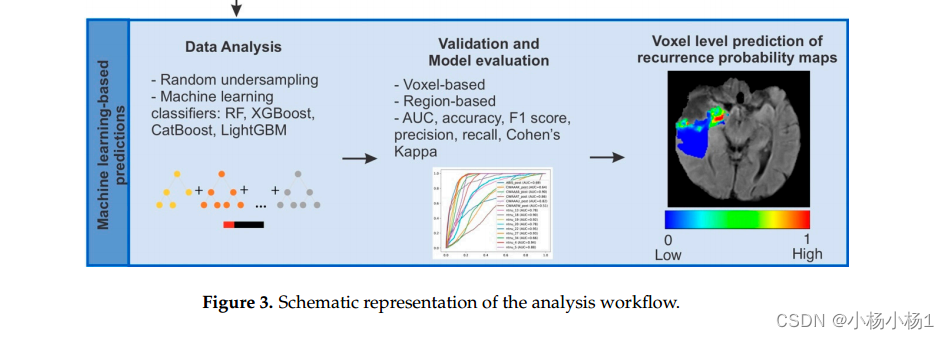
实验结果