头颈部鳞状细胞癌(HNSCC)是全球第七大癌症病因,是一种异质性恶性肿瘤,起源于上呼吸道,尤其是鳞状粘膜线。唇部、口腔和鼻腔、鼻窦、喉、鼻咽、口咽和下咽是HNSCC的受累部位。利用空间组学分析平台深入剖析组织肿瘤微环境,对深入理解HNSCC发生和进展的生物学机制、开发用于早期诊断的临床相关生物标志物具有重要的参考依据;同时结合获得的空间多组学信息和临床分层,可以更好地解读治疗策略的相关机制,帮助推进HNSCC的精准医学。下面分享两篇利用DSP空间多组学分析技术助力HNSCC肿瘤微环境研究的文章,希望对相关领域研究者有所参考。
01
案例集锦
案例1:构建口腔鳞状细胞癌嗜神经侵袭的空间转录组图谱

肿瘤大小、DOI(侵袭模式)和淋巴结转移目前被认为是口腔鳞状细胞癌(Oral Squamous Cell Carcinomas,OSCC)预后和分期的重要因素。对于临床分期为T3期或以上以及出现淋巴结转移的患者,常规推荐的治疗策略是辅助化疗。然而,高达50%的I期或II期OSCC患者,尽管处于早期阶段仍会复发,而这些患者通常没有辅助治疗的指征。因此需要其他的参数(如PNI),来帮助制定针对早期患者的临床治疗策略。然而,目前PNI的诊断标准尚不明确,并且PNI作为独立的预后指标的作用也未被证实。2021年5月发表在《Clinical Cancer Research》上题为“Spatial and Transcriptomic Analysis of Perineural Invasion in Oral Cancer”的文章,研究团队对PNI的空间转录组图谱展开研究,文章中研究团队分别用S100和Pan-CK分别对来自142例患者组织切片中的神经细胞和肿瘤细胞进行形态学标记,选择肿瘤核心和肿瘤边缘的神经细胞,评估这些神经细胞的大小(直径)以及神经细胞和肿瘤细胞的距离,并进行生存分析。然后,从中选择8例患者的组织切片,利用DSP空间全转录组技术获取与肿瘤组织相距不同距离的神经细胞的空间转录组表达谱,探究其变化的趋势,挖掘差异表达的基因并进行通路的功能分析,阐明了神经细胞和肿瘤细胞之间的相互作用,并发现癌症诱导的组织损伤能够调节神经突触的生成,并支持以神经-肿瘤距离来对PNI进行重新分类。
研究思路:
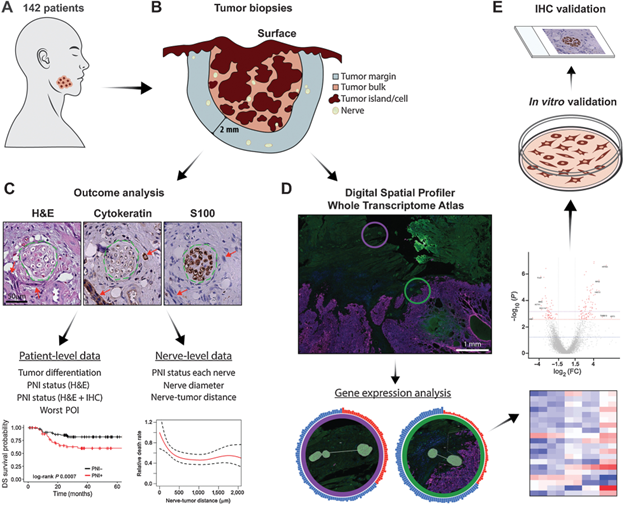
图1 研究设计的示意图

为了探索靠近肿瘤和远离肿瘤的神经之间的差异,进行DSP空间全转录组分析,对142例患者中的8例患者进行DSP空间全转录分析,根据神经-肿瘤接近程度选择感兴趣的区域(ROI),获取与肿瘤组织相距不同距离的神经细胞的空间转录组表达谱,探究其趋势变化,寻找差异表达基因和通路功能分析。

图2 OSCC的DSP数字空间全转录组分析
研究结论:
本研究首次在人类癌症中针对神经细胞进行空间转录组的分析,并发现空间转录组特征与临床结果之间存在显著相关性。这项工作阐明了神经细胞和肿瘤细胞之间的相互作用,并发现癌症诱导的组织损伤能够调节神经突触的生成,靠近肿瘤的神经细胞表现出应激响应和生长相关的基因上调。研究也提出基于神经-肿瘤距离进行重新分类,以此来作为更加充分的量化标准,从而改善患者的临床获益效果。
案例2:构建原发性和转移性口咽鳞状细胞癌患者的空间蛋白组图谱

头颈部鳞状细胞癌 (HNSCC) 通常表现为局部区域或远处疾病,尽管采用多模式治疗方法,包括手术切除、放化疗,以及最近的转移性或复发性 HNSCC 的免疫治疗。口咽鳞状细胞癌 (OPSCC) 占 HNSCC 的四分之一,在大约三分之二的OPSCC患者中,已有局部区域转移的报道。晚期淋巴结状态,尤其是结外延伸,是预后预测不良的指标,确定这些多个部位的分子表型不仅对于了解原发肿瘤很重要,而且对于了解淋巴结转移对开发有效疗法的影响也很重要。为了更深入地了解原发性和转移性组织,需要对肿瘤微环境(TME)进行研究,潜在TME生物标志物的鉴定和表征在OPSCC患者的治疗选择中具有重要的预测和预后价值。2022年5月发表在《Frontiers in Immunology》上题为“Dissecting Tissue Compartment-Specific Protein Signatures in Primary and Metastatic Oropharyngeal Squamous Cell Carcinomas”的文章,研究团队为了描述OPSCC的原发性和转移性疾病,应用数字化空间分析技术(DSP),对61例OPSCC患者的原发性肿瘤和淋巴结转移瘤样本进行68种蛋白靶标的空间蛋白分析,用肿瘤和免疫的形态学标记(PanCK:肿瘤上皮细胞;CD45:免疫细胞)绘制完整的TME蛋白图谱,探究原发性肿瘤和淋巴结转移瘤样本的差异表达蛋白,并进行生存分析。研究确定肿瘤和基质区域的特异性蛋白特征,对HNSCC和淋巴结转移的发展具有预测和预后意义。
研究思路:

为探究原发性肿瘤和淋巴结转移瘤样本蛋白的表达,研究团队利用DSP空间蛋白组学技术,对OPSCC原发性肿瘤与淋巴转移瘤样本进行68个蛋白靶标的检测,通过肿瘤和免疫的形态学标记,对肿瘤和基质区域进行划分,以鉴定匹配/不匹配OPSCC原发性肿瘤和淋巴转移瘤样本关键差异表达蛋白。
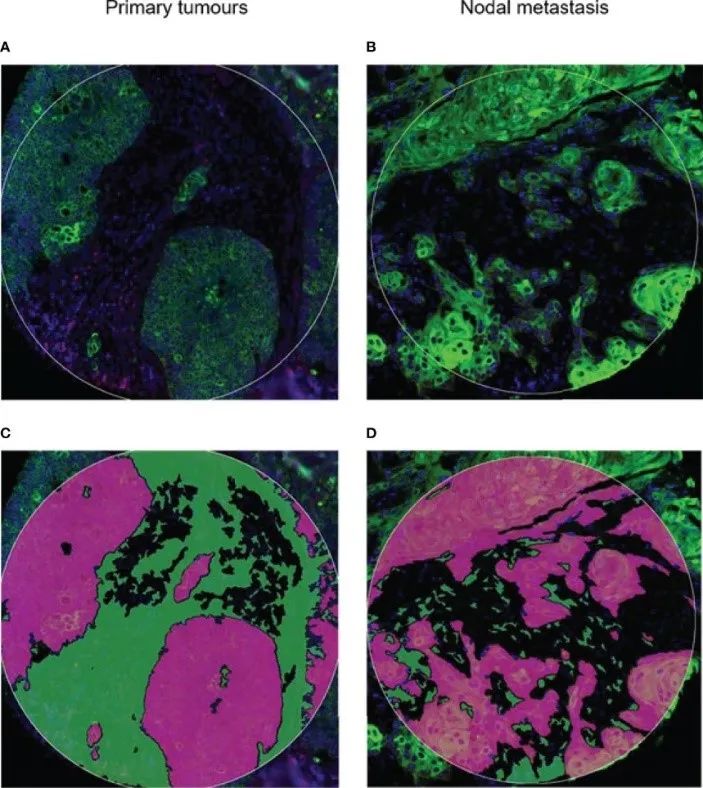
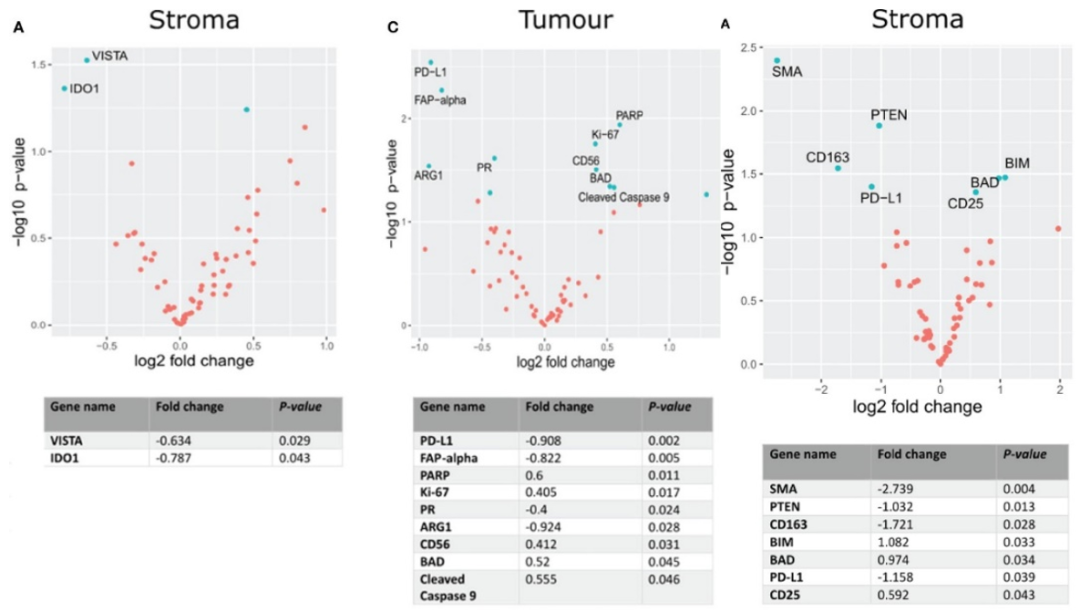
图3(A)原发性和(B)淋巴结转移的肿瘤微阵列核心进行空间蛋白组分析
研究结论:
研究确定了肿瘤和基质区域的特异性蛋白特征,生存分析表明,原发性肿瘤区域的CD25与生存率降低有关,而孕酮受体(PR)与OS改善有关,这些蛋白质特征,对HNSCC和淋巴结转移的发展具有预测和预后意义。
02
非因空间多组学研究策略
非因生物作为中国最专业、最全面的空间多组学技术服务商,一直致力于空间多组学技术的深耕和创新。目前,非因生物承接的头颈部肿瘤项目研究近十例,有丰富的头颈部肿瘤研究经验。
非因生物基于多年来积累的丰富的空间多组学研究经验,以及依靠资深的空间多组学技术专家和强大的生信分析团队,已经形成了完善成熟的空间多组学研究策略体系,以下提供部分空间组学研究策略,以辅助研究者更加充分的挖掘空间多组学数据的临床价值。