癌症转移,作为导致患者死亡的主要原因之一,其复杂机制一直是医学界研究的热点。肝脏,作为癌症转移的常见靶器官,其微环境对癌症细胞的生长和转移具有重要影响。然而,肝脏如何限制癌症转移的具体机制尚不完全清楚。
来自苏黎世联邦理工学院生物系统科学与工程系的Costanza Borrelli, Morgan Roberts, Davide Eletto 等多名研究人员发表了题为《In vivo interaction screening reveals liver-derived constraints to metastasis》的研究成果。在该文章中,研究人员使用了Y-27632(AbMole,M1817)。AbMole提供高品质抑制剂、细胞因子、人源单抗、天然产物、荧光染料、多肽、化合物库。
该研究通过体内相互作用筛选方法,揭示了肝脏对癌症转移的限制作用,并发现了一组关键基因和信号通路,为理解癌症转移机制提供了新的视角。
研究团队利用基因表达分析技术,在小鼠模型中建立了体内筛选系统。这一创新方法能够模拟癌症细胞在肝脏中的转移过程,从而筛选出影响转移的关键基因和信号通路。通过精心设计的实验方案,研究团队成功地在体内环境中捕捉到了癌症细胞与肝脏微环境之间的相互作用,为揭示肝脏对转移的限制提供了有力证据。
实验结果显示,一组肝脏特异性基因在筛选过程中脱颖而出。这些基因在肝脏微环境中表达活跃,能够显著抑制癌症细胞的转移能力。研究团队进一步发现,这些基因通过调控特定的信号通路,影响癌症细胞的生长、侵袭和迁移等关键步骤,从而实现对癌症转移的限制。
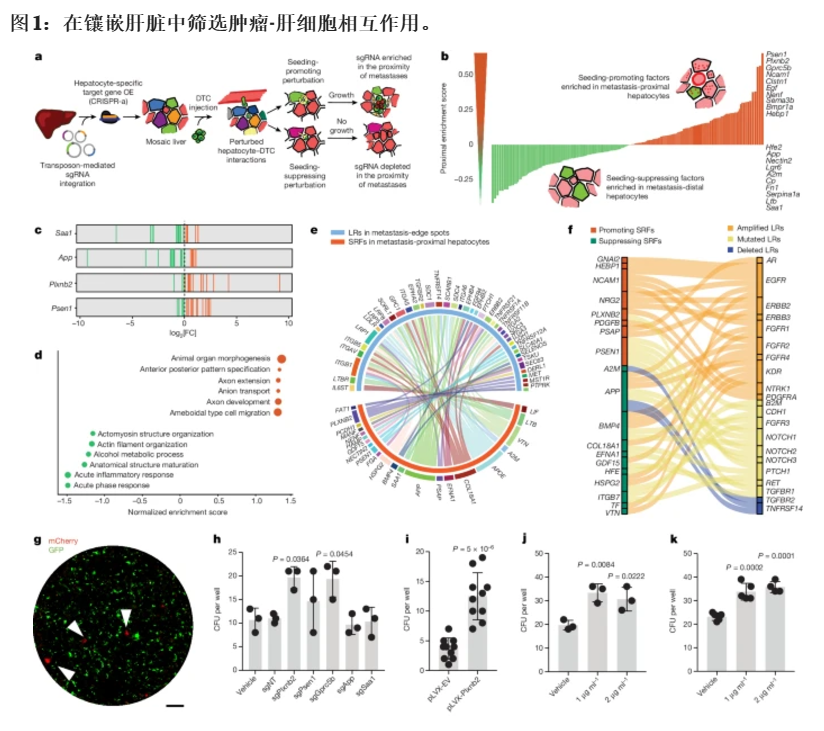
图 1:在镶嵌肝脏中筛选肿瘤-肝细胞相互作用。
特别值得注意的是,研究还揭示了多个与转移抑制相关的信号通路。这些信号通路在肝脏微环境中发挥重要作用,通过与其他细胞因子的相互作用,共同构建一个抑制癌症转移的网络。例如,某些信号通路能够调控免疫细胞的浸润和功能,增强肝脏对癌症细胞的免疫监视和清除能力;而另一些信号通路则通过影响细胞外基质的成分和结构,改变癌症细胞的生存环境和迁移路径。
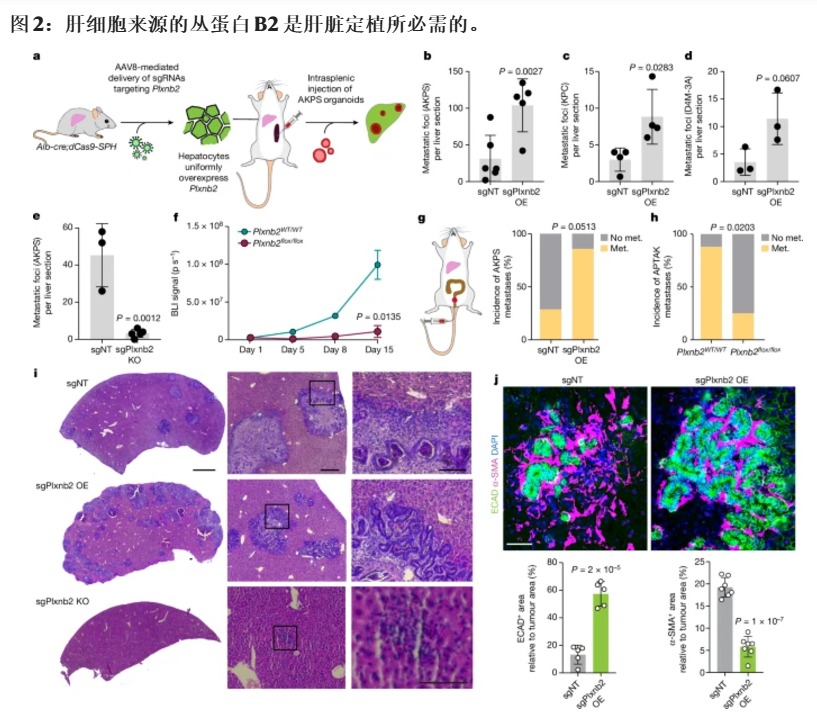
图 2:肝细胞来源的丛蛋白 B2 是肝脏定植所必需的。
肝脏微环境对癌症转移的影响是多方面的。细胞外基质作为细胞生存的基础环境,其成分和结构的变化能够直接影响癌症细胞的生长和转移。研究团队发现,肝脏特异性基因能够调控细胞外基质中某些关键成分的表达,从而改变癌症细胞的生存状态。此外,免疫细胞的浸润和代谢状态也是影响癌症转移的重要因素。肝脏微环境中的免疫细胞能够识别并清除癌症细胞,而代谢状态的变化则能够影响癌症细胞的能量供应和生长速度。
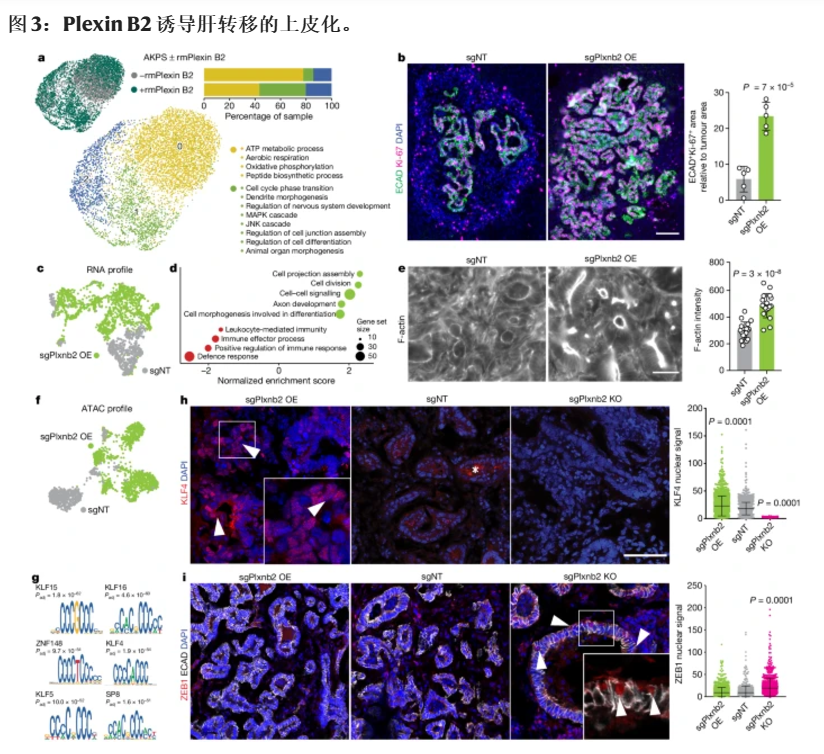
图 3:Plexin B2 诱导肝转移的上皮化。
本研究的发现对于癌症的临床诊断和治疗具有重要意义。通过检测患者体内是否存在影响转移的关键基因或信号通路异常,医生可以预测癌症转移的风险,从而为患者制定个性化的治疗方案。例如,针对某些关键基因的突变或信号通路的异常激活,医生可以选择特定的靶向治疗药物或免疫疗法,以提高治疗效果并减少副作用。AbMole(奥默生物)是ChemBridge中国区官方指定合作伙伴。
此外,研究还揭示了潜在的治疗靶点。这些关键基因和信号通路不仅为开发新的抗癌药物提供了方向,还为评估现有药物的疗效和安全性提供了新的视角。通过深入研究这些靶点的作用机制和调控网络,科学家们可以设计出更加精准和有效的治疗方案,为患者带来更好的治疗体验和生存质量。
展望未来,随着研究的深入和技术的进步,我们有望更加全面地理解癌症转移的机制,并开发出更加精准和有效的治疗方法。同时,这项研究也为个性化医疗的发展提供了有力支持,为实现癌症患者的长期生存和治愈目标奠定了坚实基础。
综上所述,本研究通过体内相互作用筛选方法揭示了肝脏对癌症转移的限制作用,并发现了一组关键基因和信号通路。这些发现不仅增进了我们对癌症转移机制的理解,还具有重要的临床意义,为癌症的预测、诊断和治疗提供了新的策略和方向。未来研究将进一步探索这些发现的临床应用潜力,并推动个性化医疗的发展。