摘要
功能磁共振成像(fMRI) block设计实验通常包括呈现认知任务的ON-block和无认知任务的OFF-block。然而,ON-block之间的OFF-block也可以看作间歇性休息的标志,从而诱发短暂的静息状态。目前仍然不知道这种间歇期的大脑活动是否反映了与连续期相同的静息态活动。因此,本研究的目的是考察间歇和连续休息条件下大脑活动的异同。共有47名健康受试者参与了3T fMRI实验。间歇静息态数据来自标准的ON-OFF block设计中活动任务处理之间的静息期,在ON-block期间呈现了三种不同的认知任务。连续静息态数据是在任务完成后的5分钟静息期间获取的。研究结果发现,两种条件下的活动总体相似,但存在一些差异。这些差异存在于默认模式网络(DMN)中,并与其他脑网络的相互作用有关。DMN图显示内侧前额叶皮层(MPFC)的条件之间具有较弱的重叠,特别是间歇静息态条件下的重叠比连续静息态条件下要弱。此外,DMN在间歇静息态条件下与突显网络(SN)具有较强的连接,特别是在前岛叶和边缘上回区域。观察到的差异可能反映了从任务处理到下一个静息状态周期的“延续效应”,这种效应在连续静息态条件下不存在。未来需要进一步的研究来充分了解间歇和连续静息态之间的差异程度。
前言
静息态功能连接的测量在神经成像领域引起了极大的兴趣,主要有两个原因:首先,研究为理解人脑提供了新的见解,包括功能连接和结构连接之间的可能重叠。其次,使用静息态数据研究功能连接相对直接,可以应用于脑发育和临床研究。与基于任务的功能磁共振成像(fMRI)等其他方法相比,这可能会提高依从性,降低训练需求。功能连接通常使用低频(<0.1Hz)血氧水平依赖(BOLD)信号波动来计算,从而推断出感兴趣区域(ROIs)之间的神经活动。这些低频波动通常在静息条件下获得,此时大脑处于休息状态。这被认为代表了自发的神经激活以及无约束的心理活动,例如“发呆”或“走神”。
静息态功能连接研究揭示了一致的大规模空间分布的相干信号,我们称之为静息态网络(RSNs)。目前已证实这些网络反映了支持核心知觉和认知过程的脑功能系统。有趣的是,尽管RSNs主要与静息期间自发出现的BOLD波动有关,但这些网络在任务范式和意识状态改变时也显示出同步波动。例如,默认模式网络(DMN)是研究得最多的RSN,在任务条件下显示出较强的相关性,但相对于静息状态下的相关性较弱。因此,根据任务中平均网络活动与刺激事件时间的相关性方向,这些网络可以被描述为“任务正网络”或“任务负网络”。一些研究表明,执行认知任务可能会对随后的静息期产生“延续效应”,从而影响RSN连接。例如,Waites等人(2005)对正字法词汇检索任务前后的静息期DMN区域进行功能连接分析发现,任务执行前后的静息期间,功能连接略微增加或减少。Pyka等人(2009)提供的证据显示,与非挑战性的字母匹配任务相比,被试在完成具有认知挑战性的工作记忆任务后, DMN活动增加。这可以解释为静息期间对前一项任务的自我评估和反思的功能性相关性,或者从挑战性认知需求中恢复的认知资源重新分配。此外,Fox和Raichle(2007)的研究表明,连贯的自发脑活动可以解释任务范式中的试次间差异。因此,得出静息期间内在神经元活动可能影响后续任务相关行为和相应脑活动的结论并非不合理。此外,Sadaghiani等人(2010)认为,正在进行的活动是以功能架构组织的。诱发的神经反应被嵌入到一个潜在的功能架构中,如果脱离了正在进行的活动所建立的背景,就无法完全理解。
这些观察结果为本研究提供了背景,本研究的重点是检查和比较单次长时间静息期获得的RSN数据和在任务处理期间重复短暂静息期获得的数据。本研究使用了标准的fMRI block设计,探索了两种静息态条件下RSN活动的相似性和差异性,即间歇静息态和连续静息态。由于默认模式网络(DMN)是最著名和研究最多的RSNs之一,因此本研究着重考察了这两种实验条件下默认模式网络的异同。本研究假设,虽然DMN活动原则上在两种条件下应该是相似的,但这些条件下显示的精神状态差异可能会影响记录的DMN活动和两种实验条件之间的连接。为了比较两种条件下的静息态数据,本研究首先从OFF-blocks中提取BOLD图像来创建间歇性静息条件数据集。其次,使用独立成分分析(ICA)从两种条件中提取RSNs,并确定DMN成分进行统计比较。第三,利用置换统计量和配对t检验比较了DMN与所选图谱网络区域的ROI-to-ROI功能连接。
材料和方法
参与者
参与者为47名健康成人,27名男性和20名女性(M=34.9岁,SD=13.9)。参与者是公开招募的,纳入标准为自我报告无任何精神和神经系统疾病。在MRI数据采集之前,研究人员与参与者进行了面谈,询问他们体内是否有植入物(如心脏起搏器)和任何幽闭恐惧症的迹象。此外,让参与者签署知情同意书。女性参与者会被问及是否怀孕,因为这是一个排除标准。本研究根据《赫尔辛基宣言》的伦理标准执行,符合良好的临床实践框架,并且符合人类研究机构的所有伦理规则和指南。本研究获得了挪威西部医学研究伦理区域委员会的批准(#2014/1641/REK-Vest)。
刺激和设计
基于任务的fMRI包括三种不同的认知任务:心算任务、工作记忆任务和心理旋转任务。实验包括九个有任务呈现的ON-blocks(每个任务重复三次)和九个无任务呈现的黑屏OFF-blocks交替进行,但视野中央有一个十字注视点。任务在每个ON-block中呈现34s,每个参与者的任务顺序不同,并与34s的OFF-blocks交替进行。在E-Prime软件(Psychology Software Tools,Inc.,USA)上进行刺激时序、持续时间、先后顺序以及实验整体时序参数的控制。刺激呈现与MR数据采集使用NordicNeurolab SyncBox(NordicNeuroLab Inc.,Norway)进行同步。要求参与者在OFF-blocks的呈现过程中保持眼睛睁开。每个ON-block和OFF-block持续68s,总计10min2s。在静息态阶段,要求参与者在扫描仪中静卧并放松五分钟。为了保持一致性,从实验的静息态阶段中获得的数据将在下文中称为“连续静息态条件数据”,而从基于任务的静息(OFF) block中提取的数据将称为“间歇静息态条件数据”。
磁共振扫描和数据采集
使用西门子3T Magnetom Prisma MR扫描仪采集数据。在功能成像之前使用以下序列参数获取解剖学T1加权图像:MPRAGE 3D T1 加权矢状面体积,TE/TR/TI=2.28ms/1.8s/900ms,采集矩阵=256×256×192,视野(FOV)=256×256mm2,200Hz/px读出带宽,翻转角8°,总采集时间为7.40min。所有fMRI数据均采用2D梯度回波平面成像(EPI)获取,采集参数如下:TE/TR=30ms/2s,间歇条件为306个volumes,连续条件为150个volumes,采集矩阵=64×64,层厚=3.6mm,35层,FOV=230×230mm。
fMRI数据处理
在任务态fMRI数据预处理前,从4D任务态fMRI图像的九个OFF-block中分别提取七个最中心的3D体积以进行进一步处理。每个OFF-block由17个体积组成,其中每个OFF-block的前五个和后五个体积被省略,以避免包含从ON-block到OFF-block的BOLD信号的瞬态波动,以及避免参与者可以预测下一个认知任务的出现。数据提取过程如下:首先使用SPM12的函数spm vol和spm read vols将间歇静息态数据分解为独立的体积。然后使用SPM函数spm write vol将感兴趣的体积保存为独立的3D nifti图像。使用collapse nii scan将提取的“静息”3D体积合并为由63个体积(总时间2分1秒)组成的4D图像。整个过程在Matlab R2017b(MathWorks,Natick,MA)中执行。
间歇静息态条件由9个ON-block和9个OFF-block组成,每个block包含17个体积(见图1)。图1中垂直的红线表示为了提取间歇静息态体积,将4D fMRI图像进行剪切的位置(由线上方的剪刀表示)。从每个OFF-block中剪出7个体积。前五个和后五个体积被省略,也就是图中所示的红色垂直线之外。将提取的OFF-block体积合并,得到由63个OFF-block体积组成的4D fMRI图像。

图1.Block设计图示。
所有预处理均在Matlab R2017b中使用CONN功能连接工具箱17b执行。预处理包括配准和畸变校正、功能数据以(0,0,0)坐标居中、功能异常值检测、功能分割和归一化、结构数据以(0,0,0)坐标居中、结构分割和归一化,以及平滑处理。
空间ICA
对两个条件下的静息态数据分别进行空间独立成分分析(ICA)。采用Group ICA for fMRI toolbox(GIFT v3.0b)进行ICA分析。对于每个条件,使用“Infomax”算法类型提取了20个独立成分,其他设置均为默认设置。提取的独立成分根据Smith等人(2009)的DMN成分图模板的相关系数进行了空间排序。这样做是为了自动选择两个数据集中最能反映DMN的成分,并获得每个条件下的网络概览。
关联分析和概率图
使用与模板DMN图相关性最高的均值参与者的成分来选择单个参与者的成分,以便在每个个体的所有相对成分图像中进行二级关联分析(单因素方差分析,随机效应)。这允许量化在两种静息态下已识别的DMN成分之间的相似性水平。采用SPM12进行关联分析(conjunction analysis)。所有相关的成分图(每个参与者和条件各一个)被纳入二阶分析(单因素方差分析)。在对模型进行估计后,定义多重对比进行比较。对统计图进行多重比较(FWE)校正,并选择p值为0.05的显著性阈值且聚类程度为10体素进行所有比较。此外,为了测试与模板DMN图相关性最高和次高的成分的空间重叠,本研究使用SPM12计算了所有成分和所有参与者的概率图。首先,使用z>1.96(相当于p<0.05)的阈值对所有成分进行二值化。其次,将所有二值化的成分按体素相加,乘以100并除以图像总数量。因此,显示的体素值表示在两种条件下所有参与者中存在最高和次高的DMN相关成分的概率(%)。
功能连接分析
本研究进行了感兴趣区域(ROI)分析,以探索DMN和所选8个网络在两种静息态条件下的功能连接差异。使用CONN工具箱进行ROI-to-ROI功能连接分析。计算属于DMN的四个ROIs之间的功能连接z值:DefaultMode.MPFC(1,55,-3),DefaultMode.LP (L)(-39,-77,33),DefaultMode.LP (R)(47,-67,29),DefaultMode.PCC(1,-61,38),以及属于CONN默认网络图谱中定义的8个选定功能网络(DMN,感觉/运动,视觉,突显,背侧注意,额顶叶,语言,小脑)的32个ROIs。进一步提取两种条件下的连接矩阵,并使用FSL中的线性模型置换分析(PALM)进行条件间比较。
结果
ICA分析
对静息态数据进行空间ICA分解,为两种条件下的每个条件生成20个独立成分图。对各成分进行空间排序后,针对每个条件选择与模板DMN图相关性最强的两个成分图,如图2、3所示。
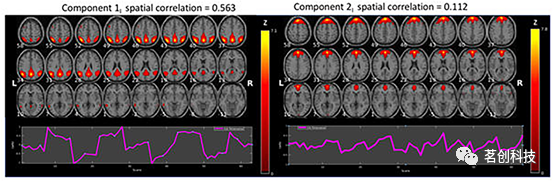
图2.间歇(I)静息态数据的ICA分析结果(z>1.96)。

图3.连续(C)静息态数据的ICA分析结果(z>1.96)。
图2显示了与Koch等人(2002)中的示例DMN图谱相关性最高的两个成分。每个成分下面是相应的时间进程。该图显示了从上(左上角)到下(右下角)以3mm的步长叠加在轴向解剖层上的BOLD激活,MNI z坐标范围为58到−11。与ICA成分1相关的ROIs位于双侧楔前叶/后扣带皮层(PCC)、顶下小叶和顶上小叶。与ICA成分2相关的ROIs位于内侧额上回,双侧外侧额上回,前扣带皮层(ACC)/辅助运动区(SMA),双侧颞中回。
图3显示了与Koch等人(2002)中的示例DMN图谱相关性最高的两个成分。同样,每个成分下面是相应的时间进程。从上(左上角)到下(右下角) 以3mm的步长叠加在轴向解剖层上的BOLD激活,MNI z坐标范围为58至-35。与ICA成分1相关的ROIs位于双侧楔前叶/后扣带皮层(PCC)、外侧额上回和内侧额上回/前扣带皮层(ACC)。与ICA成分2相关的ROIs位于楔前叶/后扣带皮层(PCC)、双侧顶上小叶和顶下小叶、双侧颞中回。
如图2、3所示,虽然这两种条件都激活了前后脑区的DMN节点,但这两种条件之间也略有不同。图2显示,间歇条件下的ICA-1I成分主要激活于后部DMN区域,ICA-2I主要激活于前部脑区。图3显示,连续条件下的ICA-1C成分主要激活于前部和后部区域,ICA-2C主要激活于后部脑区。
关联分析
使用与每个参与者模板DMN(1I-间歇静息条件和1C-连续静息条件)相关性最高的成分进行的连接分析显示出大量的空间重叠。这表明DMN在间歇和连续静息条件下都被激活,参见图4。此外,在所有47名参与者中,本研究计算了与模板DMN图具有最高和次高相关性的成分的概率图(1I和2I代表间歇静息条件和1C和2C代表连续静息条件)。概率图显示,各成分之间的重叠在DMN的额部ROI较弱,而在后部ROI区域的重叠最强,见图5。

图4.该图显示了间歇(1I)(红色)和连续(1C)(蓝色)成分的关联(绿色)分析结果。
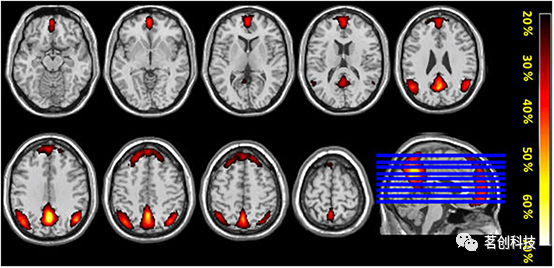
图5.显示了从两种条件(间歇静息态和连续静息态)中获得的ICA成分重叠的平均概率图(以%表示)。
功能连接分析
在这两种条件下,DMN网络ROIs与其他选定网络ROIs之间的六种连接如表1所示。有趣的是,大多数观察到的显著差异连接是在DMN网络的种子和突显网络(SN)之间(见图6)。为了更好地显示这些差异,本研究计算了Cohn’s d效应值(图7)。所呈现的效应值表明,间歇条件下DMN与其他ROIs之间的显著连接高于连续静息态条件。不同条件间的比较采用配对双尾t检验。表1显示了两种条件之间显著不同的连接[p(-log10)>1.301]。
表1.间歇和连续静息态数据的DMN ROIs比较。


图6.DMN和突显网络种子之间连接的可视化。图中所示的区域是:后扣带皮层(PCC)、内侧前额叶皮层(MPFC)、边缘上回(SMG)、前岛叶(AI)、外侧顶叶(LP)和后颞上回(PSTG)。右半球用R标记,左半球用L标记。

图7.间歇和连续静息态条件下功能连接的Cohen效应值存在显著差异。
图6所示的连接在间歇和连续静息态下均存在显著差异[p(-log10)>1.3010]。图6所示圆形图中线条的粗细表示两个条件之间给定连接的差异程度。图中所示的解剖区域是:后扣带皮层(PCC)、内侧前额叶皮层(MPFC)、边缘上回(SMG)、前岛叶(AI)、外侧顶叶(LP)和后颞上回(PSTG)。右半球用R标记,左半球用L标记。
图7显示了显著连接的Cohen’d效应值。结果表明,对于两种条件下的平均功能连接的大多数显著差异,间歇静息态条件的值高于连续静息态条件下的相应值。图7所示区域为:后扣带皮层(PCC)、内侧前额叶皮层(MPFC)、边缘上回(SMG)、前岛叶(AI)、外侧顶叶(LP)和后颞上回(PSTG)。右半球用R标记,左半球用L标记。
结论
在间歇静息态下的OFF-blocks期间观察到的DMN网络与连续静息态下获得的DMN网络具有相似的模式。但这两种条件之间也存在一些差异,主要表现在网络的额叶区域。通过DMN节点与全脑体积之间的功能连接分析,进一步揭示了两种条件之间的差异。从图7可以看出,间歇静息态下的DMN似乎与突显网络(SN)的某些部分具有明显更强的连接,先前的研究认为这些连接与调节DMN和CEN之间切换有关。观察到的差异可能反映了从任务处理ON-blocks对后续OFF-blocks的“延续效应”。然而,需要进一步的研究来充分了解这两种条件之间的差异程度,以及DMN在间歇和连续静息态下是否本质上相似。检查DMN网络在更长时间的活动和休息期间的变化动态,或者通过改变任务难度和认知负荷来考察“延续效应”是否与任务相关也很有必要。
参考文献:Beresniewicz J, Riemer F, Kazimierczak K, Ersland L, Craven AR, Hugdahl K and Grüner R (2023) Similarities and differences between intermittent and continuous resting-state fMRI. Front. Hum. Neurosci. 17:1238888.
doi: 10.3389/fnhum.2023.1238888