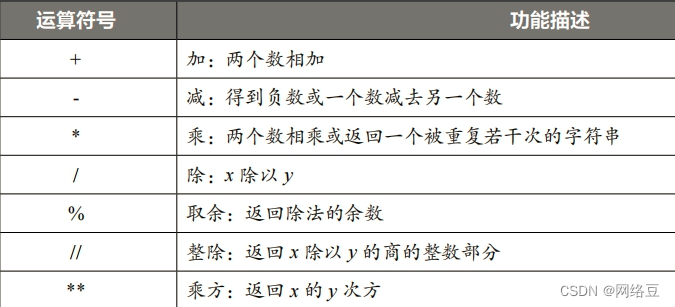
第2章:电压、电流和电阻
2.1 原子结构
- 元素:不能用化学方法分解成更简单形式的物质称为元素。
- 原子:原子是体现元素特性的最小粒子。
- 原子核:原子核由质子和中子组成,质子带有正电荷,中子呈中性。电子带有负电荷,围绕着原子核运动。质子上的正电荷和电子上的负电荷是可以彼此孤立存在的最小电荷。

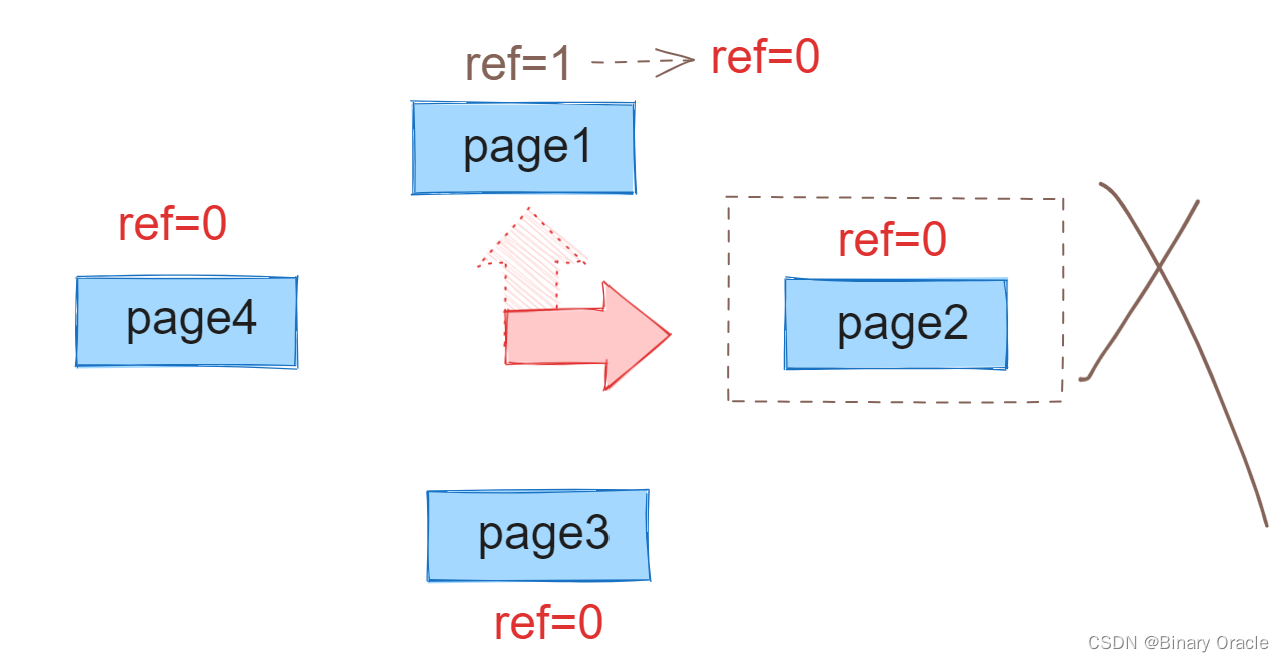
- 原子的玻尔模型,显示了在圆形轨道上围绕原子核运动的电子。电子拖着的“尾巴”表明它们在运动。
- 每个元素的原子中都有不同的质子数,据此元素之间得以区分。
2.1.1 原子序数
所有元素都按照原子序数有序地排列在元素周期表中。原子序数等于原子核中的质子数。例如,氢的原子序数为1,氦的原子序数为2。
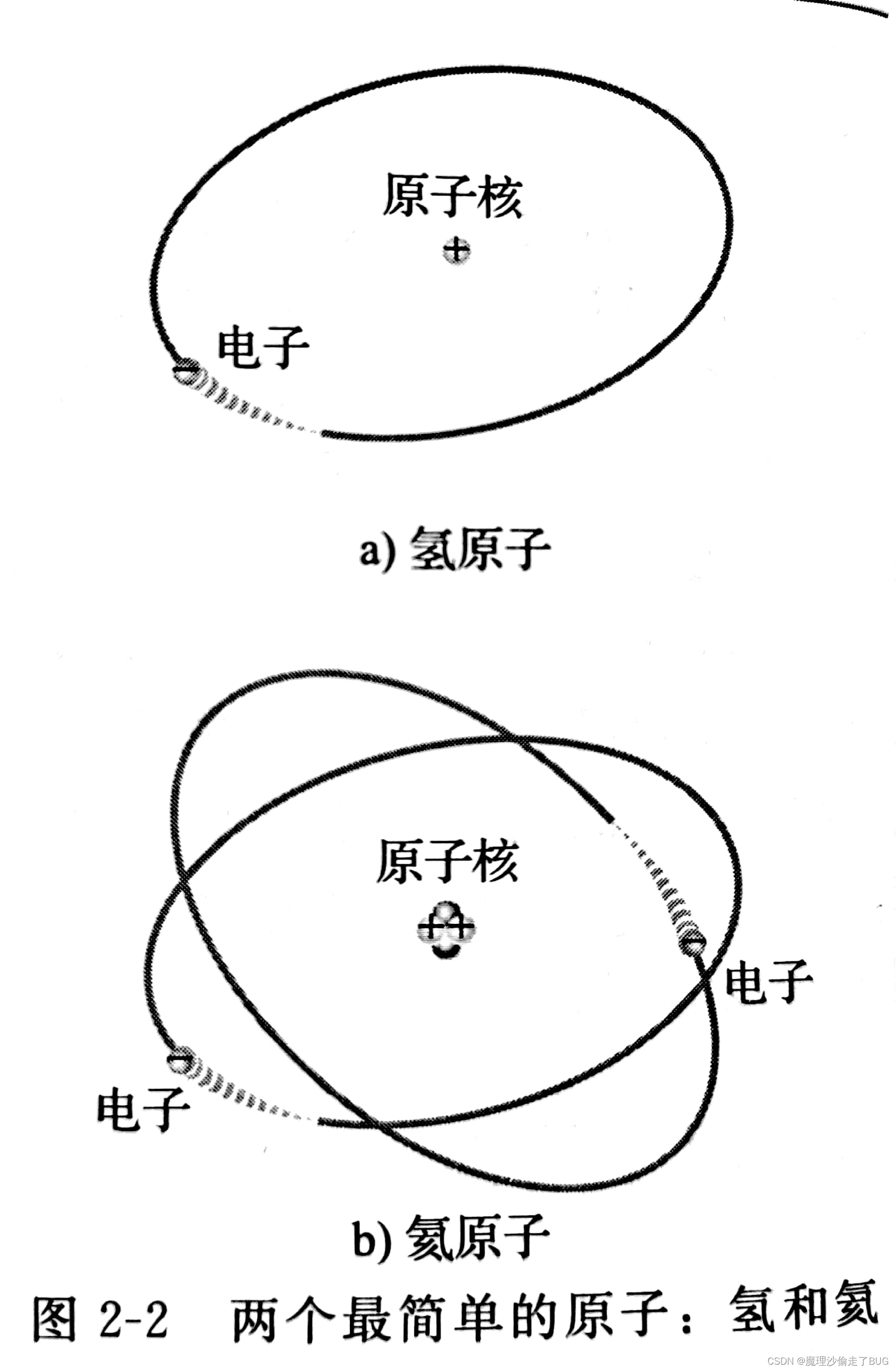
在正常(或中性)状态下,质子和电子的数量是相同的,正、负电荷抵消,整个原子呈电中性。
2.1.2 电子层、轨道和能级
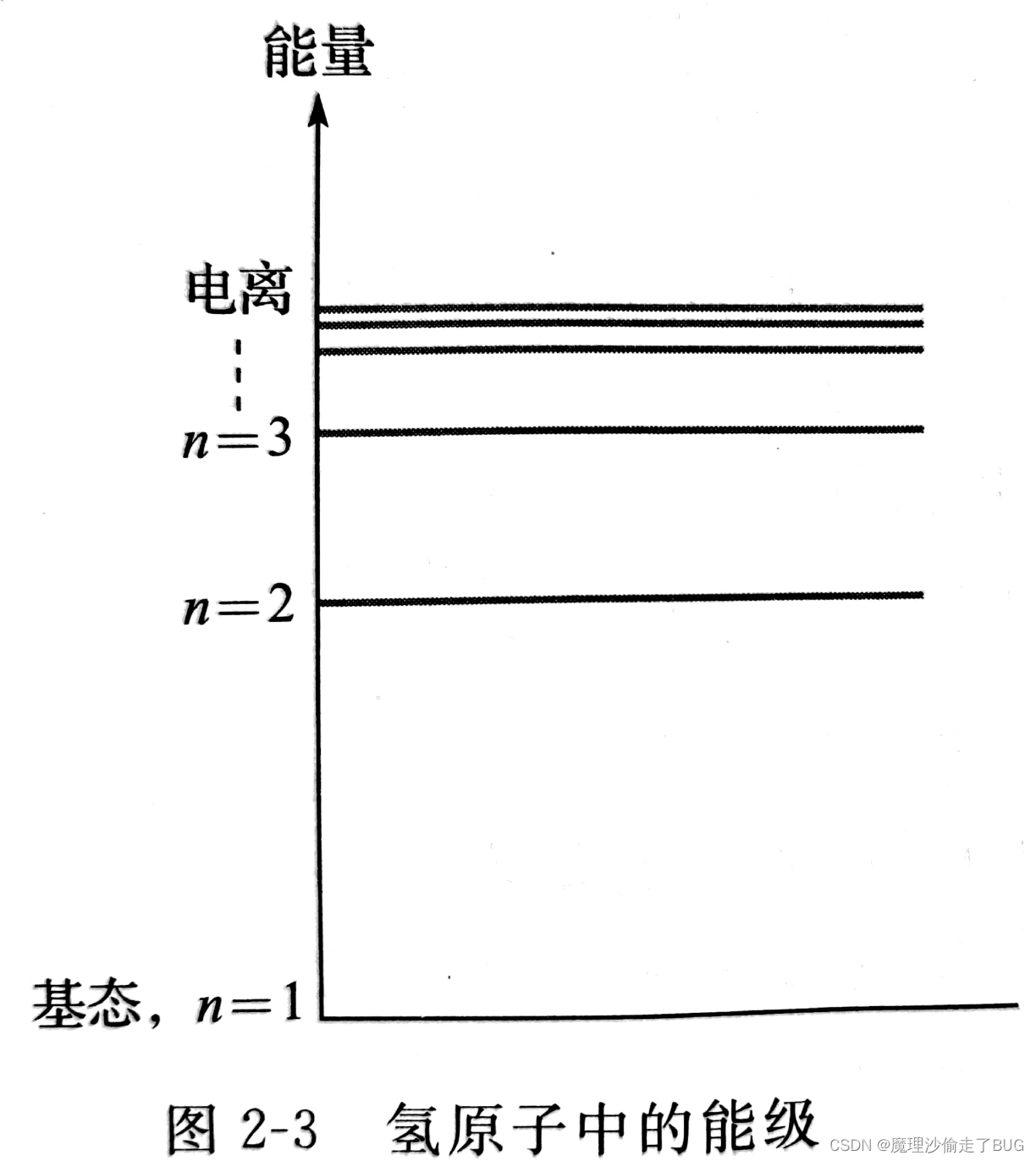
正如玻尔模型中所看到的,电子在离原子核有一定距离的特定轨道上绕着原子核运行。每一条轨道被称为一个电子层,对应院子内的不同能级。电子用1、2、3等来标注,其中1层最靠近原子核,电子越远离原子核,它的能级越高。
最底层(n=1)称为基态,对于单电子原子(氢原子)而言,仅有一个电子位于第一层时是最稳定的。
在波尔的研究之后,薛定谔提出了一种原子数学模型,该模型可以解释更复杂的原子。他认为电子具有类似波的性质,且认为最简单的情况由震动引起的三维驻波图形。原子内离散能级的概念仍然是理解原子的基础,而波动力学模型在预测各种原子的能级非常成功。原子的波动力学模型在能量方程中使用了主量子数(即电子层序数)的概念,并通过其他3个量子数描述原子内的每一个电子。一个原子内的所有电子对应着一组特定的量子数。
2.1.3 价电子
离原子核较远的轨道上的电子能量较高,与离原子核较近的电子相比,它们与原子的结合不那么紧密。最外电子层被称为价电子层,这个层中的电子被称为价电子。这些价电子在一定程度上决定了材料的化学反应性质和材料的点穴性质。
2.1.4 能级和电离能。
- 自由电子:如果一个电子吸收了一个具有足够能量的光子,它就会从原子中逃逸出来,成为一个可以在电场或磁场影响下运动的自由电子。
- 离子:对应图2-3中的电离能级。如果一个原子或一组原子带净电荷(正负电荷数目不等),则称其为离子。
- 负离子:当一个电子从中性的氢原子(记为H)逸出时,该原子就带一个净正电荷,于是编程一个正离子(记为H+)。另一方面,一个原子或一组原子也可以获得一个或多个额外的电子,在这种情况下,称其为负离子。
2.1.5 铜原子
- 铜是电气技术中最常用的金属。
- 铜原子有29个围绕原子核运行的电子,且这些电子排布在4个电子层上。
- 每个电子层上可容纳的电子数为 2 N 2 2N^{2} 2N2个,其中 N N N是电子层序数。
- 任何原子的第1个电子层最多可以有两个电子,第2层最多可以有8个电子,第3层最多可以有18个电子,第4层最多可以有32个电子。
- 铜原子的结构如图所示:
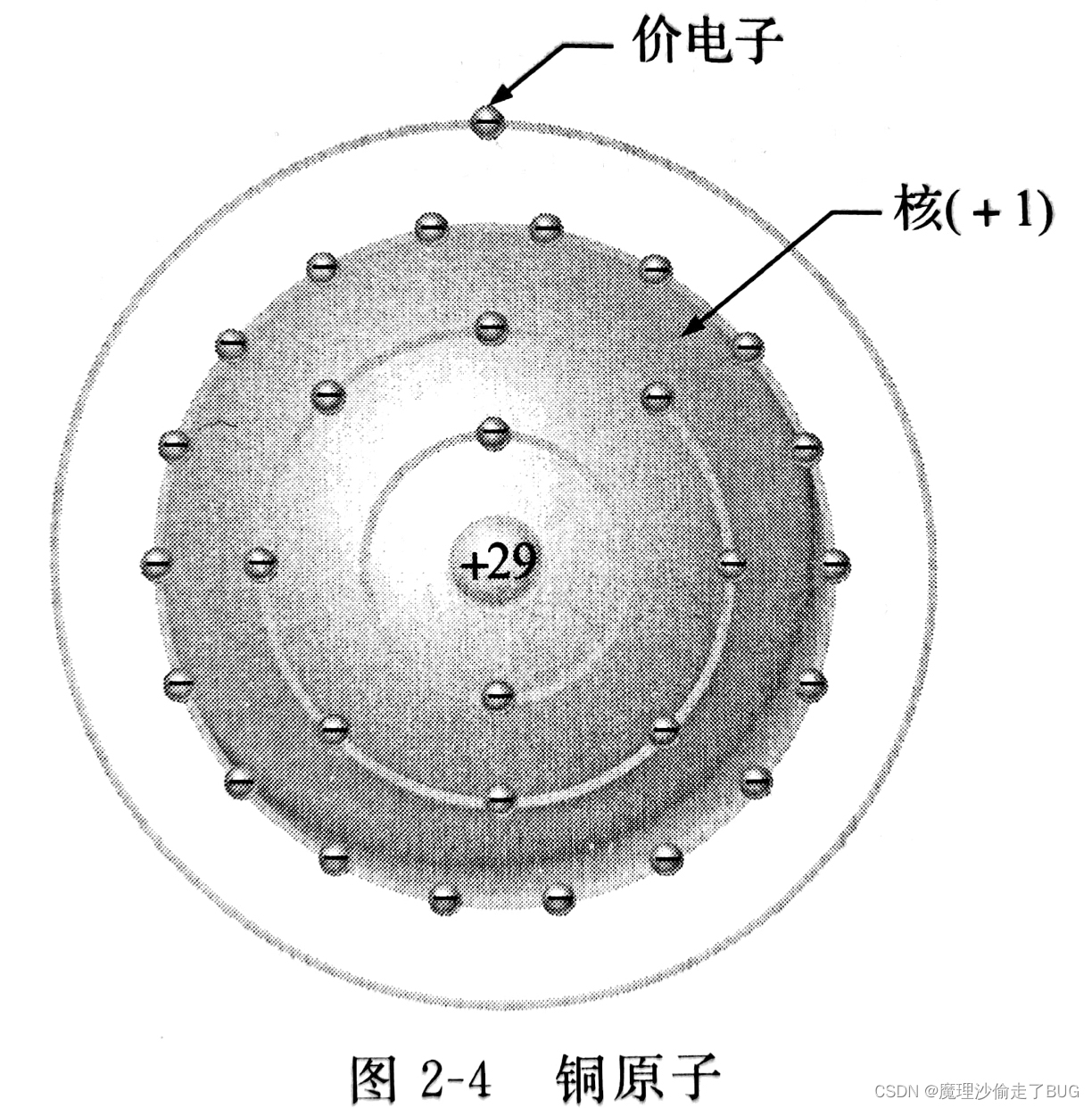
注意第4层(最外层)或者说价电子层,只有1个价电子。内部的电子层称为核。 - 当铜原子最外层的价电子获得足够的热能时,它就可以脱离所属原子而称为自由电子。这些电子不与某个特定的原子结合,可以在铜材料中自由移动。这些自由电子使铜成为极好的导体。
2.1.6 材料类别
电子工业中使用的材料有3种:导体、半导体和绝缘体
- 导体:导体是容易传导电流的材料。它们有大量的自由电子,导体结构中有1~3个价电子。
- 半导体:由于半导体的自由电子比导体少,因此其载流能力弱于导体。半导体的原子结构中有4个价电子,然而由于其独特的性能,某些半导体材料成为诸如二极管、晶体管和集成电路等电子器件的基础。
- 绝缘体:绝缘体是非金属材料,是电的不良导体。它们被用在不需要电流的地方以防止电流通过。绝缘体的结构中没有自由电子,价电子被原子核束缚,且不被视作“自由的”。
课后习题
(1)负电荷的基本粒子是什么?
答: 电子。
(2)解释原子的含义。
答:原子是体现所属元素性质的最小粒子。
(3)原子是由什么组成的?
答:原子是由带正电荷的原子核(原子核包括质子和中子),以及周围环绕着轨道运行的电子组成的。
(4)给出原子序数的定义。
答:原子序数是原子核中的质子数。
(5)所有元素都有相同类型的原子吗?
答:不是,每个元素都有不同类型的原子。
(6)什么是自由电子?
答:自由电子是脱离所属原子后的外层电子。
(7)原子结构中的电子层是什么?
答:电子层是电子围绕原子核运动的能带。
(8)请说出两种导电材料。
答:铜和银。