大脑皮层包含六层结构,美国精密神经科学公司(Precision Neuroscience Corporation)的研究人员提出了第7层皮层接口:可拓展的微创脑机接口平台。构建了一种模块化的和可拓展的脑机接口平台,包括高通量薄膜电极阵列和微创手术植入系统,促进与大脑皮层表面的大部分区域的双向通信。
脑机接口有可能恢复、替代或增强在各种疾病状态下丧失或受损的神经功能,包括由中风或脊髓损伤导致的瘫痪、失明和某些形式的认知障碍等。而现有的脑机接口依赖于侵入性的外科手术或穿透电极,这限制了该技术的应用和符合条件的患者数量,世界上只有少数患者通过临床试验获得了高度定制的接口。

研究人员认为植入手术的发病率、脑组织受损或被破坏的程度应被最小化,而不应随着植入电极的数量和密度的增加而增加。同样,植入所需的总时间应该根据电极的数量以有利的方式进行优化。研究人员构建了一种新型脑机接口平台,包括薄膜电极阵列和微创手术输送系统。这套系统可将超过2000个微电极同时植入到哥廷根小猪大脑两个半球的多个功能区,无需开颅手术,有效植入速度快于40ms/通道,且不损伤大脑皮层表面。该平台旨在通过安全、高效的方式,提供高微电极通量和高空间密度,并与神经外科技术兼容,以促进先进的、高性能的脑机接口技术的临床应用。
# 系统概述
该系统用于体内神经记录和刺激,将模块化的薄膜微电极阵列,通过一种新的“颅骨微缝”技术,进行快速、微创的硬膜下植入,即每个微电极阵列的电缆穿过硬脑膜切口和颅骨微缝切口,再穿过头皮,连接到独立的头部接口。每个微电极阵列包括529个电极,直径从20到200µm,有效面积为每529通道模块0.48 cm2。
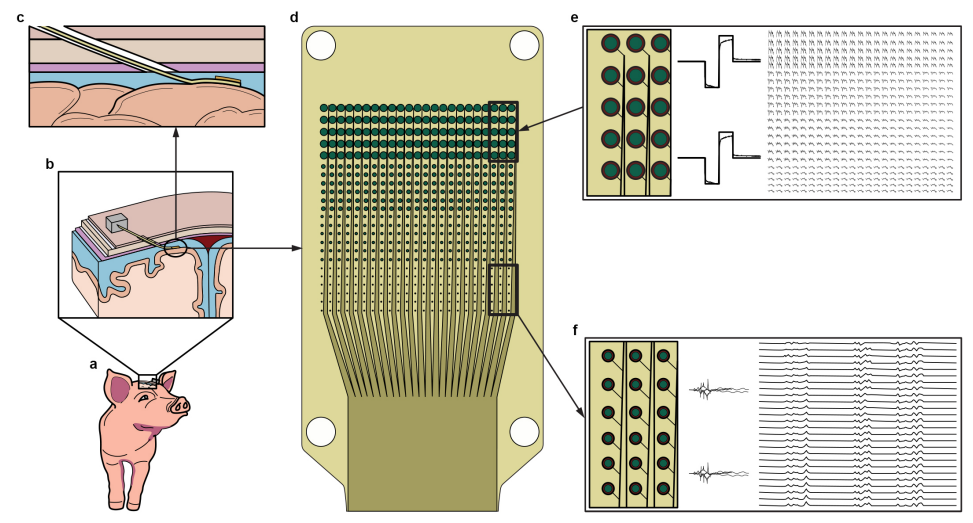
图1 整个系统配置图(硬脑膜下腔为蓝色,硬脑膜为紫色,颅骨为米色,最外层为头皮)。
# 电极阵列表征
研究人员对8个阵列的4232个微电极进行阻抗表征,其中电极连通率> 93%。在1 kHz时的阻抗幅度随着电极尺寸的减小而增大。其中,20µm直径电极的平均阻抗为497 kΩ,200µm直径电极的平均阻抗为32 kΩ。电极阵列在植入过程中具有鲁棒性,植入前后的阻抗变化很小。
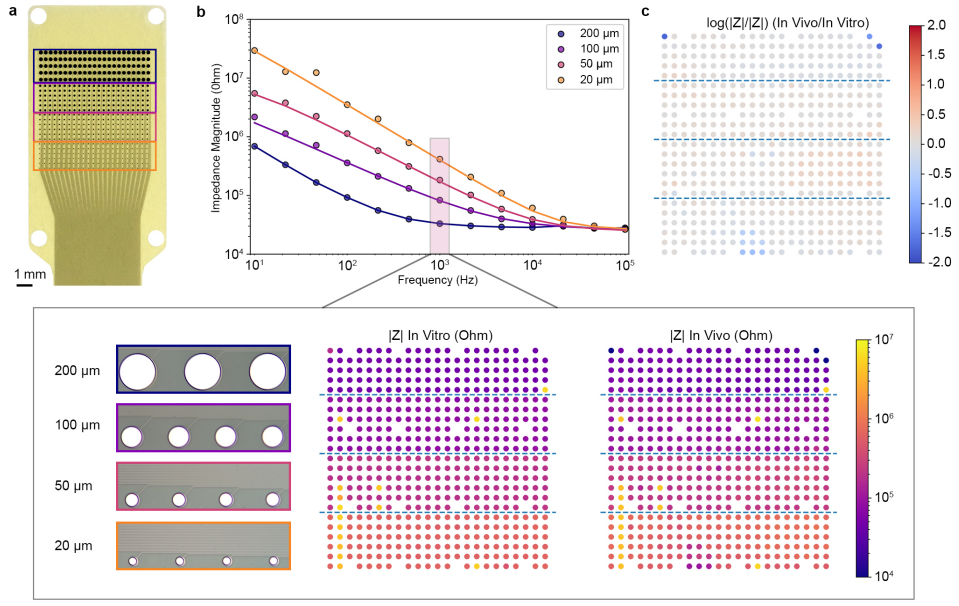
图2 电极特性
# 最小的侵入性和速度
新型微创“颅骨微缝”技术。采用精密的振荡刀片在颅骨上以与皮层表面切向的角度做400微米宽的切口,而不需要钻孔或开颅手术。电极阵列安装在一个加强垫片上(垫片插入到阵列背面(顶部)的聚酰亚胺中,形成5.5mm*11.5mm的口袋),在实时成像和纤维内窥镜的引导下,通过颅骨狭缝,植入硬膜下空间,卸下垫片,将电极阵列留在脑区。颅骨和硬脑膜切口后的电极植入时间为20-40s。对于单个阵列的529个微电极,这相当于每个微电极在0.48 cm2皮层上的平均植入速率< 40-80 ms。
# 安全性和可逆性
在阵列移除后,软脑膜保持完整,没有发现皮质表面有组织被破坏。
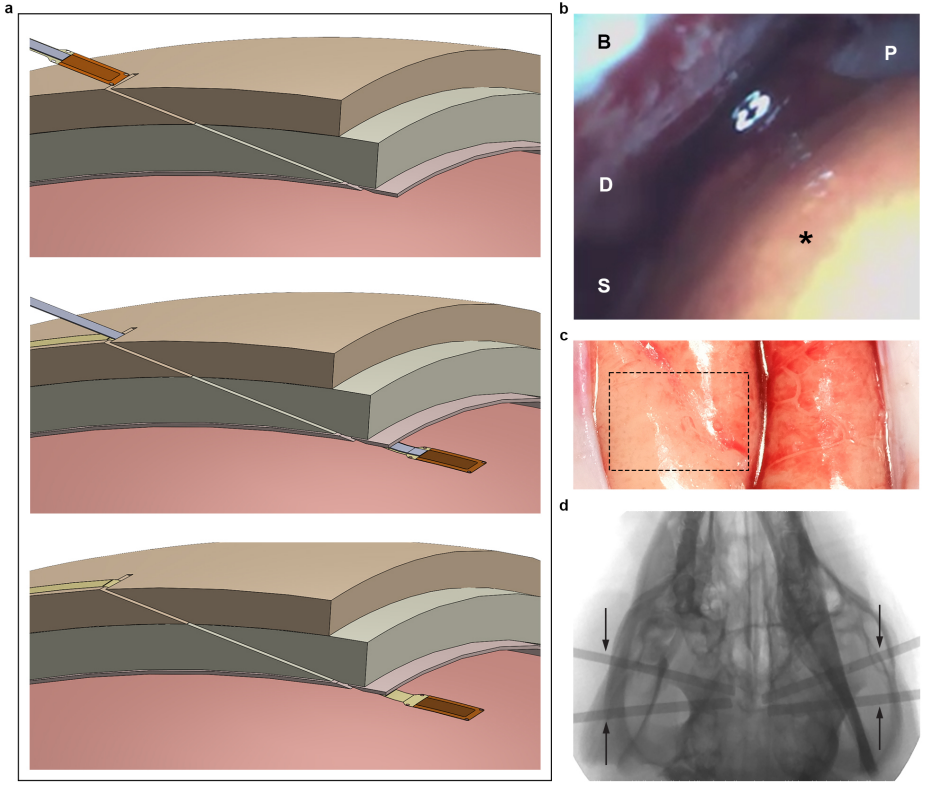
图3 插入技术
# 模块化和可拓展性
阵列便于模块化组装。多个电极模块可以连接起来,产生更大的结构,覆盖皮层表面的更大空间,而不会显著增加阵列插入所需的复杂性、风险或时间。可以通过一个狭缝插入多个阵列。在体内插入双连接模块(1058个通道,皮层表面积超过0.96cm2),在体外插入四层连接模块(2116个通道,皮层表面积超过1.92 cm2)。使用双连接模块会使有效平均插入速率减半,达到了每个电极< 20ms的有效速度。

图4 模块化和可扩展性
# 神经记录
植入阵列用于多通道神经记录,捕获躯体感觉皮层的自发神经电活动(图5b)以及体感诱发电位(与左后肢的触觉刺激相对应)(图5e)和视觉诱发电位(对左眼视网膜进行光刺激,由一个白色发光二极管阵列以1 Hz产生周期性的50 ms闪光)(图5f)。
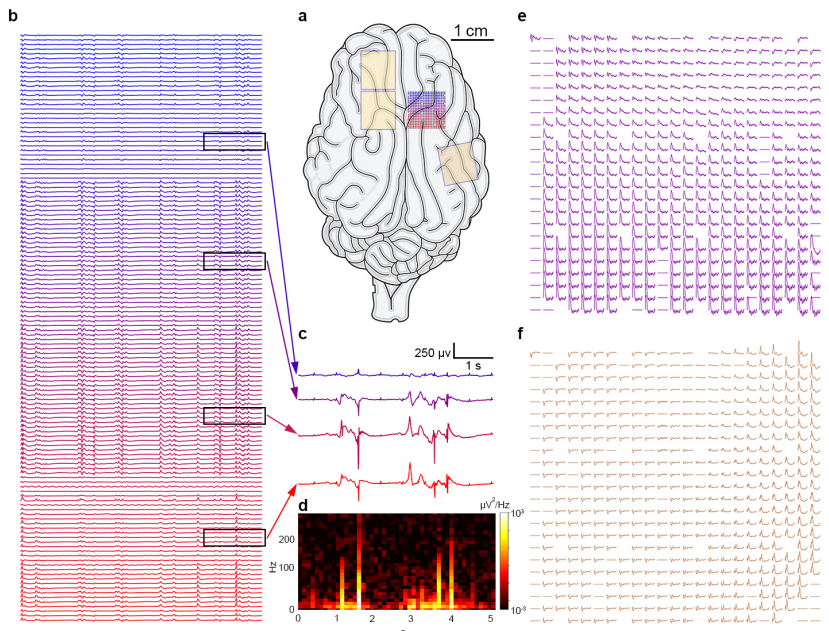
图5 神经记录
# 神经解码
研究人员分析了从给定阵列的参考位点记录的自发神经活动与同一阵列上其他位点同时记录的神经活动的相关程度。发现相关性的程度随着距离的增加而降低(图6a),并随着频率的增加而降低(图6b)。重要的是,在高频下,即使是紧密间隔的电极也表现出不完全相关的活动。研究人员使用一种非加权模板匹配算法(unweighted template-matching)作为区分无刺激和对左眼或右眼刺激的基础。对整个阵列中大量电极的多通道解码比对任何单个电极解码更鲁棒,在离线解码中,左侧正确率达到73%,右侧正确率达到67%。
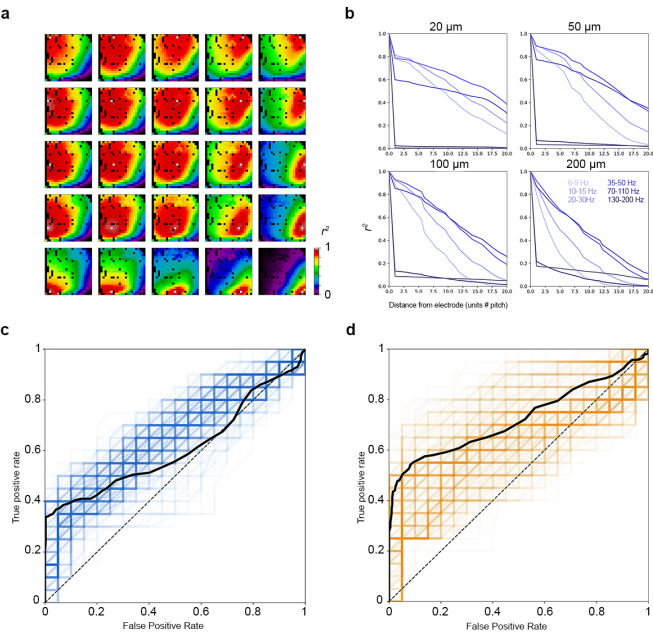
图6 解码
# 神经刺激
靶向神经刺激是闭环脑机接口以及恢复视觉等功能的神经假肢的关键功能。研究人员将电极阵列以微创的方式进入视觉皮层,刺激皮层表面,并监测刺激诱发的皮层活动。其中,每个阵列有16个电极被指定用于皮层刺激。在体外确定电极的安全刺激阈值。通过CV测量确定水窗约为1.85V(0.65V阴极和1.2 V阳极极限),并在预期的刺激参数范围内对测试电极施加50 Hz的双相脉冲,以确认安全刺激。每相50,000个10 nC脉冲和100,000个20 nC脉冲(分别为50µA和100µA,脉冲宽度为200µs),不会引起测试电极的阻抗变化和水窗内的极化电位变化,所以在这个范围内的刺激电流被认为可在体内使用(每个电极30个脉冲)。在体内进行皮层刺激,每次试验中使用200µm电极进行刺激,其余所有位点进行记录。皮层刺激在电极阵列监测的周围区域诱发了高伽马波段功率的增加,持续约1秒。最活跃的区域形成一个半径约1毫米的环,但并不是直接围绕刺激电极。远离环状区域处虽然对刺激有反应,但表现出更少的诱发活动。
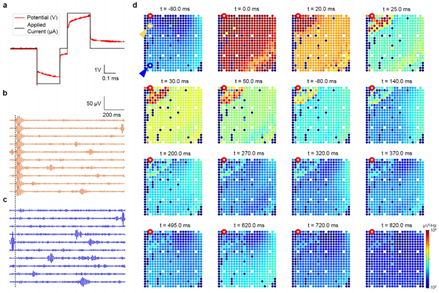
图 皮层刺激
论文信息:
The Layer 7 Cortical Interface: A Scalable and Minimally Invasive Brain–Computer Interface Platform
—— End ——
仅用于学术分享,若侵权请留言,即时删侵!
更多阅读
格拉斯哥大学中国博士生提出计算鬼成像架构
专家观点:最近Neuralink FDA IDE的真正含义是什么?
植入式脑机接口技术的医疗器械之路
LMDA-Net第一作者亲自讲述其设计思想
伸手运动想象训练与伸手抓取想象的关系

加入社群
欢迎加入脑机接口社区交流群,
探讨脑机接口领域话题,实时跟踪脑机接口前沿。
加微信群:
添加微信:RoseBrain【备注:姓名+行业/专业】。
加QQ群:913607986
欢迎来稿
1.欢迎来稿。投稿咨询,请联系微信:RoseBrain
2.加入社区成为兼职创作者,请联系微信:RoseBrain


一键三连「分享」、「点赞」和「在看」
不错每一条脑机前沿进展 ~