作为Linker的dPEG
研究证明,通过交联剂将不同物质结合在一起的能力已被证明是诊断和药物输送系统中非常有用的一项技术。由多分散PEG组成的交联剂已被用于制备多种多聚物以及将靶向配体偶联到纳米颗粒上。这通常用于需要非常大的尺寸以提供良好的DMPK性能并且受多分散性影响较小。然而,一些特性,如靶结合或细胞内化,可能会受到大尺寸的不利影响,进而对PEG链长度变化的治疗敏感性也会有所差异。但是,更小的均一dPEG则可以解决这些难题。由小烷基组成的传统交联剂(如SPDP, SIAB, SMCC, EMCS等)多年来也一直是用于生物偶联的支柱,但随着共轭设计变得更加复杂,它们固有的疏水性也导致其应用受到限制。例如,当多个实体分子共轭在一起或进行接近性分析时,连接剂成分对克服固有的疏水性至关重要。虽然有几种烷基连接剂能够以磺化形式存在,可以提高较小的连接剂的水溶性,但它们在较大结构中的应用中仍然存在问题。此外,多种带负电荷的磺酸盐也可能会导致非特异性相互作用。
dPEG产品将烷基连接物的精确性以及PEG的生物相容性结合在一起,没有任何疏水缺陷,具有高度的灵活性,并且其拥有多种独特的结构来确定结构-功能关系并优化偶联性质。在下面的例子中,Vector Laboratories展示了dPEG linker的独特优势。如需购买Vector Laboratories公司产品,咨询产品技术问题,欢迎联系Vector Laboratories授权代理商欣博盛生物。
【小分子偶联物(Small molecule conjugates)】
有研究证明了使用dPEG将小分子与诊断显像剂连接起来的优势。例如,当用2 kDa PEG、1 kDa PEG或dPEG24交联剂制备荧光素标记的叶酸二聚体时,具有dPEG24交联的二聚体表现出最高的细胞摄取量。在另一项关于多肽多聚体的研究中,PCMA靶向配体的两种二聚体通过两种均一的PEG4 linker与DOTA结合,提供了一种四聚体,比二聚体和单体结合物具有更好的药代动力学特点(PK)和肿瘤靶向性。
【多肽偶联物(Peptide Conjugates)】
研究表明,dPEG间隔剂(dPEG spacers)可以改善多肽药物偶联物的性能。例如,可以通过使用dPEG4间隔剂提高RGD-隐霉素偶联物的溶解度。此外,dPEG4还可以促进RGD-Glu-MMAE偶联物的有效载荷释放。
【寡核苷酸偶联物(Oligo Conjugates)】
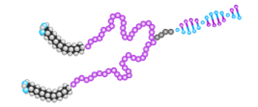
目前,寡核苷酸药物的递送是限制其应用的主要障碍之一。因此,科研工作者们研发设计了多种基于PEG交联剂的提送系统用于寡核苷酸偶联物的递送,包括抗体偶联物,肽偶联物和脂质偶联物。例如,有多种脂质-寡核苷酸偶联物(lipid-ON conjugates),包括线性和SideWinder®型dPEG4间隔剂,可用于调节药代动力学表现和跨膜递送。
【降解物和降解物偶联物(Degraders and Degrader Conjugates)】

邻近诱导降解(Proximity-induced degradation)是一种很有前景的新方法,可用于对无法药物治疗的靶点进行药物治疗的研究,且PROTACs是较受欢迎的降解物之一。连接酶和目标蛋白的配体之间的连接物通常是烷基linker或短而均一的PEG4 linker,它们在PROTAC的开发中起着关键作用。通过优化dPEG的长度可以实现高效的降解,并且一些基于dPEG的linker有助于设计“可点击”的PROTAC,从而更快地优化配体组合。
【片段偶联物(Fragment Conjugates)】
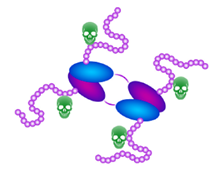
目前,正在研发中的片段偶联物有望克服与抗体大尺寸相关的研究难点,例如抗体药物扩散性和肿瘤组织穿透力差等。由于抗体片段的尺寸较小,连接体linker的特性可以在修饰偶联物的性质方面发挥更大的作用。例如,使用不同长度的dPEG间隔剂将靶向双特异性抗体的TAG72与DOTA进行交联。dPEG48间隔剂能够增加双特异性抗体的流体力学体积,从而减少肾脏清除率,提高肿瘤摄取。其中dPEG48间隔剂提供最高的肿瘤/肾脏比率。Vector Labs的SideWinder®交联剂也被证明对diabody-TCO-MMAE偶联物有益,其中较小体积的生物制剂需要正交PEG修饰剂来防止TCO触发物在体内失活。
如需购买Vector Laboratories公司产品,咨询产品技术问题,欢迎联系Vector Laboratories授权代理商欣博盛生物。
【抗体偶联物(Antibody Conjugates)】
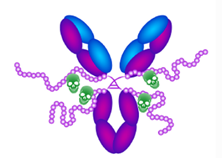
抗体偶联药物(ADC)利用dPEG间隔剂的特性来抵消疏水性有效载荷的不利影响,并改善PC、PK、BD和毒性。虽然线性dPEG交联剂提供了疏水性降低的有效载荷(例如,特西林),但类Sidewinder™的交联剂已被证明可以增加肿瘤摄取,减少脱靶摄取,并提高ADC对各种有效载荷的耐受性。此外,有研究证实,类BodyArmor™ linker还可以提供额外的结构变量,用于控制有效载荷保护和酶介导的有效载荷释放。
【纳米颗粒偶联物(NP Conjugates)】
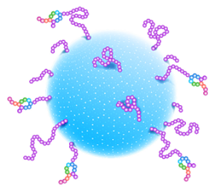
纳米颗粒通常通过被动靶向改善药物递送,目前正在探索通过连接靶向目标实现主动靶向。传统而言,这一方法是通过多分散的PEG交联剂实现的,但抗原结合和细胞内化都受到PEG涂层和交联剂中EO单位数量的影响。在一项关于靶向胶束和脂质体的研究中发现,使用不同长度的dPEG交联剂连接整合素或HER2靶向肽,细胞内化取决于dPEG长度、靶向抗原和纳米颗粒的类型。只有dPEG才能优化具有这种粒度的靶向纳米颗粒的的性能。
dPEG在化学和生物学的十字路口
总而言之,dPEG技术是众多生物偶联疗法和临床诊断分析的基础。众多研究已经展示了基于dPEG linker的实用性,并阐述了这种交联剂优越的靶标特异性,其能够改善肿瘤摄取并具有更低的毒性。使用dPEG作为连接剂(linker)、改性剂、嵌段共聚物或功能标签的优势在于它的离散性,这是传统PEG所不具备的。
Vector Laboratories拥有深厚的技术专长和制造能力,可以帮助您设计和开发独特的基于dPEG的产品,以便将其运用到您的偶联方案中。通过BioDesign服务,我们可以为您提供个性化的专家指导咨询,将您的生物偶联疗法提升到一个新的水平。如需购买Vector Laboratories公司产品,咨询产品技术问题,欢迎联系Vector Laboratories授权代理商欣博盛生物。
文献引用
① Giese M.W., Woodman R.H., Hermanson G.T., Davis P.D., et al. (2021). Chapter 9: The Use of Uniform PEG Compounds in the Design of ADCs. The Royal Society of Chemistry, ch. 9, 286-376. [The Royal Society of Chemistry]
② Tiberghien A.C., Levy J.N., Masterson L.A., Patel N.V., Adams L.R., Corbett S., Williams D.G., Hartley J.A., Howard P.W., et al. (2016). Design and Synthesis of Tesirine, a Clinical Antibody-Drug Conjugate Pyrrolobenzodiazepine Dimer Payload. ACS Med Chem Lett., 7(11), 983-987. [PubMed]
③ Giese M., Davis P.D., Woodman R.H., Hermanson G., Pokora A., Vermillion M. et al. (2021). Linker Architectures as Steric Auxiliaries for Altering Enzyme-Mediated Payload Release from Bioconjugates. Bioconjugate Chemistry, 32(10), 2257-2267. [ACSPub]