谷禾健康

在漫长的历史中,一种神秘而令人不安的疾病一直困扰着人类,那就是癫痫。
癫痫是最常见的神经系统疾病之一,影响着全世界近7000万人。它会导致突发性的、不可控制的、反复发作的痉挛和意识丧失。
突如其来的发病行为,不仅让患者和他们的家人感到恐惧和困惑,也给他们的生活带来了巨大的不便和影响。
虽然二十世纪以来出现了大量抗癫痫药物,但许多的癫痫患者对药物治疗没有反应,并且病情仍然不受控制。

近年来,动物研究和人类病例的证据表明,肠道微生物群与癫痫有关。
本文将带大家初步认识癫痫这一疾病,并阐述了肠道微生物群如何在癫痫患者和动物模型触发、加重或调节这种疾病的病程。
此外,肠道微生物群可以用作癫痫诊断和预后的潜在生物标志物以及难治性癫痫患者的新治疗靶点。
目录

Part1
初步认识癫痫
癫痫(epilepsy)是大脑神经元突发性异常放电,导致短暂大脑功能障碍的一种慢性疾病。
▼
癫痫的类型
▸ 根据发病特点分类
•全面性癫痫
涉及到整个大脑的神经元异常放电。这种类型的癫痫通常会导致全身抽搐和意识丧失。
常见的全面性癫痫包括肌阵挛性癫痫和失神癫痫等。
•局灶性癫痫
起源于大脑的一部分区域,只涉及到局部神经元的异常放电。这种类型的癫痫可能会导致局部肌肉抽搐、感觉异常或意识丧失。
常见的部分性癫痫包括颞叶癫痫和顶叶癫痫等。
▸ 根据病因分类
•继发性癫痫
继发性癫痫是由已知的病因或病变引起的。这些病因可以是脑部的结构异常、脑损伤、感染、代谢紊乱、中毒、药物副作用等。
注:继发性癫痫可以发生在任何年龄。
•特发性癫痫
特发性癫痫是指没有明确病因或病变可以解释的癫痫。在这种情况下,癫痫发作的原因可能是由于遗传因素、发育异常或其他未知因素引起的。
注:特发性癫痫通常在儿童或青少年时期开始,且没有明显的脑部结构异常。
▼
癫痫的症状
由于异常放电的神经元在大脑中的部位不同,而有多种临床表现。

✦全面性发作
这种类型的癫痫患者,往往在发作初期就会失去意识,完全意识不到自己发生了什么。
如下细分不同类型还会有各自对应的特点:
•强直-阵挛性发作
患者在发作早期,不仅失去意识,而且还会跌倒。此时患者大多会尖叫一声,全身抽搐,持续10~20秒后,发生阵挛。每一次的阵挛都会有一个间歇期,发作频率逐渐变慢、间歇期也越来越长。
在一次剧烈阵挛后,发作停止。这时候会观察到患者的瞳孔散大,唾液分泌物等增多,以及呼吸停止。之后患者会慢慢恢复,上述体征逐渐恢复正常,整个过程大概5~15分钟,有些患者在发作期还会发生牙关紧闭和大小便失禁。
患者醒来后,一般会觉得头痛,全身酸痛,很想睡—觉。
•强直性发作
此类型的患者多见于弥漫性脑损伤的患者。发作时可能是局部或全身的骨骼肌强烈而持续的收缩,能将患者固定于某一个特殊的姿势。
•阵挛性发作
此类型主要多见于新生儿和婴儿,发作时患儿会意识丧失。
•失神发作
意识丧失突然发生并迅速终止,是本类型癫痫发作的主要特征。患者可能会突然间活动停止,发呆、手上拿着的东西滑落到地板上,对旁人的呼叫无应答。也有些患者可能机械重复原有的简单动作。
•肌阵挛性发作
这是—种突然发生的类似于触电—样的不自主运动,发作时间一般比较短暂。
•失张力发作
这一类的患者往往会突然跌倒,也有些不太严重的患者会突然间低头,以及胳膊突然间下垂。
•伴有或不伴失神的眼肌阵挛性发作
此类患者的发作主要与眼部相关,大多在持续的光线下眼睑闭合后发生,间歇性的闪光刺激也可能诱发癫痫发作。发作时,患者的眼睛看起来半开半闭,有时候还会伴有手部的抽动。
✦局灶性发作
这—类的患者在癫痫发作时神志清楚,发作后能描述刚刚自己发生了什么。
一般分为以下几种类型:
•局灶性运动性发作
患者癫痫发作时,主要是某一个身体部位的不自主抽动,大多是一侧眼睑、口角、手或者足趾,也可能是一侧面部或肢体。严重的话,患者在发作过后可能发生短暂性的肢体瘫痪。
有些患者还会出现与人体的运动系统相关的异常动作,诸如不自主地重复发作前的单词或者单个音节,伴有身体或眼睛的旋转等。
•局灶性感觉性发作
这—类患者发作时,往往存在感觉异常。诸如味觉、嗅觉、听觉的异常,出现幻觉等。
•自动症
这一类的主要特征是患者出现存在意识障碍,会做一些看起来有目的,但实际上没有目的的动作,比如反复咀嚼、反复搓手或无目的地开门、关门等,发作后无法回忆起发作细节。
提醒
癫痫发作期千万不要强行约束患者,以免自己被误伤,也避免造成患者骨折、脱臼。
▼
癫痫的发病率
癫痫是一种常见的神经系统疾病,全球范围内都有发病。根据世界卫生组织统计,全世界有超过6500万癫痫患者。癫痫的发病率在不同地区和人群之间有所差异。
★ 中低收入国家癫痫发病人数较高
在高收入国家,癫痫患病率约为每1000人6.4例,年发病率为每100000人中出现67.8例。在低收入和中等收入国家 ,这些数字几乎翻了两倍。其中约80%的患者生活在中低收入国家。
中国癫痫的发病率在5‰~7‰之间,全国有650万~910万患者。每年,我国会有40万~60万人被新确诊为癫痫患者。
★ 青少年和老人易发癫痫
癫痫可发生在各个年龄人群,但儿童患者和老年患者比较常见。儿童和青少年是癫痫的高发人群,其中大约有一半的癫痫病例在20岁以下发病。
此外,在孕期女性中,癫痫发作的比例约为0.3%~0.7%。
▼
癫痫的风险因素
✦结构性病因
结构性病因是指神经影像学上的异常发现,合理推断导致患者癫痫发作,并与电子临床评估或临床发现一致。
结构性病因的原因包括缺氧缺血性脑病、中风、外伤和感染。在结构性病因中,值得注意的是在内侧颞叶癫痫发作中相对频繁地发现海马体硬化。
✦遗传性病因
癫痫被认为受到遗传的影响。一项研究发现977个基因与癫痫有关。
这些基因包括癫痫基因(引起癫痫或以癫痫为核心症状的综合征的基因)、神经发育相关的癫痫基因(与大脑发育畸形和癫痫相关的基因)、癫痫相关基因(与身体或其他方面相关的基因)。
与此相关的基因有SCN2A、SCN8A、SCN3B、KCNJ3、KCNJ10、KCNN3、KCNMB3、CACNA1H、AQP4。
基因如CACANA1A、CACNG3、CACNB4、CHRNA4、GRM4、LGI1、ASIC1a、STX1B、SYN2、SLC12A5 ME2、ALDH5A、Il-1β和IL-1RA以及GABA-A和GABA-B受体基因直接或间接影响神经递质的合成或释放,导致兴奋性和抑制性神经递质的不平衡,导致神经元过度兴奋。
影响癫痫的一些基因

Thakran S,et al.Int J Mol Sci.2020
✦感染性病因
中枢神经系统感染是癫痫的主要危险因素,也是世界某些地区最常见的癫痫病因。据报道,发达国家中枢神经系统感染幸存者人群中无端癫痫发作的风险为6.8%至8.3%,中低收入国家的风险更高。
例如囊尾蚴、人类免疫缺陷病毒、巨细胞病毒、弓形虫、结核分枝杆菌和恶性疟原虫等都会感染中枢神经系统。
✦代谢性病因
一些代谢性疾病可表现为细胞变性和髓鞘形成障碍以及神经元迁移障碍,通过对细胞或器官功能产生负面影响而间接促进癫痫发生。
尽管大多数代谢性癫痫都有遗传基础,但有些可能是后天获得的,例如吡哆醇依赖性癫痫发作和脑叶酸缺乏症。
✦免疫性病因
当不明原因的癫痫患者神经特异性抗体血清呈阳性并且有自身免疫介导的中枢神经系统炎症的证据时,可以怀疑其免疫病因。
根据基于人群的研究,自身免疫性癫痫的发病率约为所有癫痫的5-7%。这种病因的识别具有治疗意义,因为自身免疫性脑炎引起的癫痫发作应该通过免疫疗法而不是传统的抗癫痫药物疗法来治疗。
免疫反应也与癫痫的诱发和癫痫的发展有关。癫痫脑中的先天性和适应性免疫反应均由常驻免疫细胞及其分泌的介质以及从外周渗透的白细胞激活。致病性神经炎症过程可以是外周起源的,也可以是中枢起源的。外周炎症通过离子和谷氨酸稳态的变化以及促炎分子从外周炎症灶迁移到血脑屏障来增强癫痫放电。
Part2
肠道微生物群与癫痫
回顾了越来越多的临床前和临床证据,表明肠道微生物群会影响癫痫。

Amlerova J,et al.Int J Mol Sci.2021
动物实验
// 肠道菌群失衡增加了癫痫的易感性
研究人员发现,将肠道微生物群从长期应激的老鼠身上移植到幼年老鼠身上会促进癫痫的发作。这表明肠道菌群失衡,尤其是在慢性压力的影响下,增加了对癫痫的易感性。
实验结果表明,接受来自癫痫动物的微生物群的小鼠比对照组更容易出现癫痫持续状态,这表明微生物群介导了癫痫发作的易感性。
还有研究人员预测,移植癫痫小鼠的微生物群可能会通过增加健康小鼠的大脑兴奋性来诱发癫痫。
// 肠道炎症会增加癫痫发作
对肠道炎症与癫痫之间关系的进一步研究表明,肠道炎症会增加癫痫小鼠的癫痫发作活动。由此推断:肠道炎症可能是癫痫控制的有效目标,也可能是癫痫易感患者癫痫发作的一个因素。
// 益生菌降低了癫痫的严重程度
研究了益生菌混合物对大鼠戊四氮触发的大脑攻击活动、认知能力以及总脑组织抗氧化能力的影响。
结果表明,益生菌大大降低了癫痫发作的严重程度。同时,口服益生菌也部分改善了大鼠的空间学习和记忆。
虽然神经递质的抑制/兴奋以及抗氧化剂和氧化剂之间的失衡是癫痫发作的主要原因,但益生菌治疗增加了γ-氨基丁酸活性并改善了大鼠抗氧化剂和氧化剂之间的平衡。
微生物群-肠-脑轴与癫痫
微生物群-肠-脑轴由中枢神经系统 、肠神经系统和 肠道微生物群构成,通过向上传导和向下传导进行通信。
// 健康的肠道菌群会产生良好的代谢产物
不良的肠道菌群会上调促癫痫代谢物的产生、炎症因子的分泌等,导致γ-氨基丁酸/谷氨酸比例异常,进而诱发癫痫。
慢性压力可能是这一过程的触发因素。
健康的肠道微生物群可以产生良好的代谢产物,例如短链脂肪酸和血清素,可以抑制癫痫的发生。下丘脑-垂体-肾上腺轴、肠神经系统和迷走神经系统也参与肠道菌群与癫痫之间的相互作用。
癫痫中的微生物群-肠-脑轴

Ding M,et al.Front Immunol.2021
重点来了
具体地说,对于癫痫,癫痫发作和癫痫发生可能会受到肠道微生物群通过以下方式的影响:
1) 肠道产生神经递质,如γ-氨基丁酸、谷氨酸和血清素;
2) 通过免疫系统介导的促炎作用,释放细胞因子和趋化因子,以及脂多糖水平的增加,导致肠和血脑屏障通透性增加和神经炎症增加;
3) 通过改变肠道源性代谢物的量,例如主要以中枢神经系统保护作用而闻名的短链脂肪酸。
此外,神经和神经内分泌下丘脑-垂体-肾上腺轴,以及内源性大麻素系统和脑源性神经营养因子的水平可以受肠道微生物群干扰癫痫发作机制的影响。
癫痫患者的肠道微生物群
已经有多项关于癫痫患者和健康对照之间肠道微生物群差异的临床研究。
但目前人体临床研究主要关注两个方面:一是癫痫患者肠道菌群与健康人的差异,二是癫痫患者服用益生菌或粪菌移植后症状的改善。
本文主要采用了华西医院神经内科的研究,该研究的样本量较大,纳入55名被诊断确认超过三年的癫痫患者和46名来自同一家庭的健康对照。
与不生活在同一家庭的人相比,夫妻之间的肠道细菌群落往往更加相似。因此,我们在研究的探索和验证队列中纳入了健康配偶作为对照。仅包括一起生活并饮食相似至少10年的夫妇。



Gong X,et al.Front Microbiol.2020
此外,该研究中还排除了一些可能影响癫痫的风险因素,使结果的可信度更高。
癫痫患者和健康对照的排除标准如下:(1)最近3个月内接受过抗生素、益生菌、益生元或合生元治疗;(2)近3个月内有胃肠炎病史;(3)有其他自身免疫性疾病史(多发性硬化症、视神经脊髓炎、系统性红斑狼疮、类风湿性关节炎、1型糖尿病等);(4)肠道手术史;(5) 怀孕或哺乳期;(6)有神经或精神疾病史(帕金森病、阿尔茨海默病、焦虑症、抑郁症、自闭症谱系障碍、精神分裂症等);(7)6个月内除抗癫痫药物外的其他方案摄入史(维生素、蛋白质、不饱和脂肪酸等);(8) 严重营养不良或感染或吸毒或酗酒。
研究结果
// 癫痫患者的肠道微生物α多样性下降
通过使用 16S rDNA 测序,发现癫痫患者组的α多样性指数远低于健康对照组。最近,相对较低的微生物多样性与儿童药物难治性癫痫以及与中枢神经系统改变相关的其他疾病有关,包括阿尔茨海默病、多发性硬化症和帕金森病。
// 梭杆菌等具有致病性作用的菌群在癫痫患者中过度生长
结果表明,一些细菌门,包括梭杆菌(Fusobacteria)、疣微菌(Verrucomicrobia)和硝化螺旋菌(Nitrospirae),在疾病组中生长过度。而厚壁菌门和Saccharibacteria在疾病组中数量较少。
梭杆菌
现有研究表明,梭杆菌对脊椎动物具有致病性,在人类结直肠癌和发炎的肠道粘膜中普遍存在。一些研究人员将梭杆菌属物种描述为病原体,因为它们具有侵入性,并且能够转移到血液中并导致全身疾病状态。
疣微菌
疣微菌门以大量产生短链脂肪酸和粘蛋白降解的微生物而闻名。疣微菌可以降解粘蛋白,这可能会扰乱肠道屏障的完整性以及随后的细菌易位。
硝化螺旋菌
硝化螺旋菌可以增加亚硝酸盐的毒性,最终可能导致血脑屏障功能障碍和通透性增加,并有助于癫痫的作用机制。
拓展:A. muciniphila过高的危害
在我们的检测中发现一名56岁女士肠道内该菌的丰度占比超50%,菌群构成如下:

过量的Akkermansia将过度消耗粘液蛋白而存活下来,这是大多数其他细菌所缺乏的生存优势。
在这种情况下,非粘液消耗物种的数量显著减少,导致物种多样性减少, Akkermansia增殖异常,从而可能导致肠道屏障损伤,诱发肠道炎症、脂多糖进入血液的增加、自身免疫性疾病、神经退行性疾病等有关。
// Blautia、双歧杆菌等菌属丰度增加
预后不良的患者中,经黏液真杆菌属(Blautia)、双歧杆菌属、Subdoligranulum、普雷沃氏菌(Prevotella)、戴阿利斯特杆菌属 (Dialister)和Anaerostipes增加。
较高丰度的普雷沃氏菌会引发炎症
普雷沃氏菌为肠道核心菌,但是较高丰度的普雷沃氏菌会促进炎症。较高丰度的普氏菌可能导致肠道中持续产生IL-6,从而引发炎症反应。此外,据报道,普雷沃菌属会改变肠道通透性。
扩展阅读:肠道重要基石菌属——普雷沃氏菌属 Prevotella
癫痫患者碳水化合物代谢增加可能导致双歧杆菌丰度较高
此外,我们研究中的功能分析还显示,疾病组的碳水化合物代谢显著增加。已经确定碳水化合物代谢物的紊乱可能在癫痫发生机制中发挥潜在作用。双歧杆菌消化复杂的碳水化合物并表现出最大的预测糖生物组之一。
// 耐药性癫痫与药物敏感性癫痫患者的肠道微生物也不同
此外,耐药性癫痫患者的肠道微生物组可能与药物敏感性癫痫患者不同。
与药物敏感性癫痫患者相比,耐药性癫痫患者的α多样性和主要属于厚壁菌门的细菌的相对丰度有所增加。
注:在难治性癫痫组中,粪肠球菌(Enterococcus faecalis)、长双歧杆菌(Bifidobacterium longum)和迟缓埃格特菌(Eggerthella lenta)是潜在的生物标志物。
还有一些关于癫痫患者肠道微生物群的其他研究,主要研究成果展示在下表:


Ding M,et al.Front Immunol.2021
小结
这些研究表明肠道微生物群与癫痫之间有着千丝万缕的联系。肠道微生物群的组成可能会影响癫痫的易感性。
需要注意的是,癫痫患者之间的差异以及所使用的研究方法存在局限性。考虑到影响肠道微生物组的变量较多,如年龄、饮食和生活环境等的差异,需要在合理控制变量的基础上进行更大样本的分析。
Part3
微生物群-肠-脑轴与癫痫的相关机制
▼
免疫和炎症途径
癫痫的发病机制与神经免疫和神经炎症有关。越来越多的证据表明,脑肠轴的免疫和炎症通路可能参与癫痫的发病机制。
小胶质细胞和星形胶质细胞是中枢神经系统中主要的炎症细胞,其炎症状态会促进癫痫的发生。
√肠道微生物群通过调节免疫影响癫痫
肠粘膜的淋巴组织含有体内所有免疫细胞的70%–80%。
肠道微生物群会影响免疫细胞:例如,无菌小鼠表现出免疫异常,T细胞和B细胞数量减少,细胞因子产生减少。
此外,肠道微生物群似乎是小胶质细胞成熟以及星形胶质细胞激活的最重要因素之一。肠道微生物群调节先天免疫、适应性免疫和炎症机制,以调节癫痫的发展。
√肠屏障和血脑屏障损伤影响大脑
肠粘膜屏障和血脑屏障共同作用,防止肠道微生物群及其分泌物进入大脑。
“肠漏”综合征的特点是肠道通透性增加,导致细菌、有毒代谢物和小分子转移到血液中。在肠道炎症下,细菌可以直接将因子释放到体循环中,从而激活外周免疫细胞,改变血脑屏障完整性,从而改变转运速率,甚至可以诱发“漏脑”。
压力会增加肠粘膜通透性,管腔内的脂多糖和其他细胞因子进入血液循环刺激Toll样受体,产生炎症细胞因子,增加血脑屏障通透性并损害大脑。
√神经免疫与癫痫的发生
小胶质细胞和星形胶质细胞通过释放过量的细胞因子参与癫痫的发病机制,并相互作用。
星形胶质细胞是大脑中最丰富的神经胶质细胞,具有多种功能,包括调节血脑屏障的完整性、神经递质的循环利用以及参与免疫反应。
小胶质细胞是中枢神经系统的常驻巨噬细胞,介导先天免疫反应。
小胶质细胞和星型胶质细胞相互作用的机制
小胶质细胞可以调节星形胶质细胞的表型和功能,例如小鼠小胶质细胞可以通过VEGF-B(促进星形胶质细胞的致病反应和炎症反应)和TGF-α(促进相反的反应)来调节星形胶质细胞的行为。
肠道微生物将膳食色氨酸代谢为芳基碳氢化合物受体激动剂,并与其受体相互作用,控制小胶质细胞活化以及TGF-α和VEGF-B表达,从而调节星形胶质细胞的致病活性。
星形胶质细胞释放的炎症细胞因子和趋化因子增强小胶质细胞的活性,包括迁移、凋亡细胞的吞噬作用和突触修剪。
血脑屏障通透性增加易引起神经炎症
星形胶质细胞和小胶质细胞之间的相互作用导致促炎细胞因子的产生和血脑屏障通透性增加,从而导致外周血免疫细胞和细胞因子渗入中枢神经系统,以及随后的慢性神经炎症。
无菌和抗生素处理的动物也改变了小胶质细胞的形态以及成熟、激活和分化方面的缺陷,导致对多种病原体的免疫反应不足,而这种免疫反应可以在肠道微生物群重新定植后修复,这表明肠道微生物多样性对于小胶质细胞和中枢神经系统功能至关重要。
肠道微生物群通过先天免疫诱发癫痫
肠道微生物群可以通过先天免疫途径诱发癫痫。在无菌小鼠的整个生命周期中,血脑屏障通透性不断增加,这与内皮细胞中occludin和claudin-5蛋白表达的降低有关。
肠道微生物群失调会减少紧密蛋白的产生并增加肠壁的通透性,导致微生物、代谢物和毒素从肠腔中逸出。肠道微生物群失调还会减少短链脂肪酸,从而增加血脑屏障通透性并促进神经炎症。
如果这两个屏障被打破,微生物群释放的免疫细胞和炎症因子就会进入大脑并诱发癫痫发作。
肽聚糖是细菌细胞壁的成分,主要存在于人体肠道中。肽聚糖作为慢性脑炎的驱动因素,也在大脑小胶质细胞中检测到。因此,我们得出结论,肽聚糖可能通过促进肠漏和脑漏从肠道转移到中枢神经系统,导致慢性炎症并诱导癫痫的发生。
肠道微生物群通过适应性免疫促进癫痫的发生
肠道微生物群还通过诱导适应性免疫来促进癫痫的发生。肠道微生物群可以诱导免疫细胞产生细胞因子,通过肠粘膜和血脑屏障进入大脑,激活大脑免疫细胞参与免疫反应。
辅助T细胞17(Th17)是是适应性免疫的关键组成部分,IL-17是由Th17细胞产生的细胞因子,可以通过特定的肠道微生物群(例如拟杆菌门)进行调节。
最近发现,癫痫患者的脑脊液和外周血中IL-17水平均高于对照组,并且与癫痫发作的频率和严重程度高度相关。因此,肠道微生物群可以通过介导IL-17影响癫痫的发生。
此外,共生微生物群的缺失会下调IgA和IgG1,并上调 IgE,从而导致疾病易感性增加。
因此,肠道微生物群可以通过肠-脑轴诱导免疫反应,从而导致癫痫发生。
然而,只有少数研究直接关注肠道、免疫反应和癫痫之间的关系,许多问题仍有待探索。
▼
神经系统
在大脑和肠道之间传递信息的重要途径之一是通过自主神经纤维。
√肠道刺激通过自主神经系统调节大脑活动
给小鼠口服空肠弯曲杆菌会导致脑干迷走神经感觉神经节和初级感觉中c-fos表达增加,表明肠道刺激可以通过自主神经系统调节大脑活动。
√神经足细胞与迷走神经元接触影响神经系统
迷走神经刺激已成为癫痫的常规治疗方法。据报道,迷走神经传入纤维的电刺激可以改变大脑中血清素、γ-氨基丁酸和谷氨酸的浓度,从而解释了其在癫痫中的用途。
以前,肠道内分泌细胞和脑神经被认为只能通过激素进行交流;然而,最近发现称为神经足细胞的肠内分泌细胞可以与迷走神经元突触,以转导肠腔信号,使用谷氨酸作为神经递质将肠腔连接到脑干。
神经足细胞的发现为通过调节肠道微生物群来治疗神经系统疾病提供了强有力的理论支持。
▼
肠内分泌信号和微生物代谢物
√肠内分泌信号和神经递质与癫痫密切相关
神经递质失衡与癫痫密切相关。癫痫病灶存在神经递质失衡,如γ-氨基丁酸活性低下、谷氨酸活性亢进、多巴胺和去甲肾上腺素活性亢进、血清素活性低下。
肠道微生物影响神经递质的产生
在胃肠道中,神经递质可由肠道微生物群直接分泌或由胃肠细胞在肠道微生物群代谢物的刺激下产生。
不同的肠道微生物群可以产生不同的神经递质(肠球菌属、链球菌属和埃希氏菌属产生血清素;乳杆菌属和双歧杆菌属产生γ-氨基丁酸;埃希氏菌属和芽孢杆菌属可以产生多巴胺)。
肠道微生物群产生的各种神经递质可以通过肠粘膜,但很少通过血脑屏障,γ-氨基丁酸除外。在海马损伤或癫痫状态下,肠道微生物群产生的γ-氨基丁酸会导致γ-氨基丁酸和谷氨酸系统之间的不平衡,从而引起癫痫发作。
一些肠道菌群调节氨基酸水平从而影响癫痫
嗜黏蛋白阿克曼菌(Akkermansia muciniphila)和Parabacteroides定植可以改变血清和肠腔中的氨基酸水平,从而调节海马中与癫痫发作相关的神经递质(例如 GABA 和谷氨酸)的水平,从而为小鼠提供保护性抗癫痫作用。
血清素可以改善癫痫患者的发作
肠嗜铬细胞产生大约90%的血清素。在小鼠中,某些肠道微生物群,例如形成孢子的梭菌类群,可以通过上调结肠色氨酸羟化酶1(一种血清素生产的限速酶)来促进肠道中血清素的生物合成。
先前的研究表明,颞叶癫痫患者存在血清素缺乏症。增加血清素的药物组合,例如选择性血清素再摄取抑制剂,可以改善癫痫患者的癫痫发作控制。
去甲肾上腺素对癫痫发作具有双重作用
去甲肾上腺素对癫痫发作具有双重作用,具体取决于其含量,低剂量的去甲肾上腺素具有促癫痫作用,而高剂量的去甲肾上腺素可以抑制癫痫。
√短链脂肪酸癫痫密切相关
短链脂肪酸包括乙酸盐、丙酸盐和丁酸盐,可以由一些肠道细菌(主要是拟杆菌属和厚壁菌门)通过不溶性膳食纤维的发酵产生。
短链脂肪酸在小胶质细胞成熟、肠脑神经系统、血脑屏障通透性以及通过直接或间接途径的应激反应中发挥着重要作用,所有这些都与癫痫密切相关。
不同短链脂肪酸对癫痫的保护作用
在癫痫小鼠模型中进一步研究了不同短链脂肪酸对癫痫的保护作用和机制。
丁酸盐可能通过减轻肠道炎症和氧化应激,表现出抗癫痫作用。丁酸盐还可以通过Keap/Nrf2/HO-1途径改善线粒体功能障碍并保护脑组织免受氧化应激和神经元凋亡的影响,从而提高癫痫阈值并降低癫痫强度。
丙酸盐治疗可以通过减少线粒体损伤、海马细胞凋亡和神经缺陷来减轻癫痫发作强度并延长癫痫发作潜伏期。
这些研究表明,短链脂肪酸在癫痫模型中减少,并且通过不同的机制对癫痫具有保护作用。
▼
下丘脑-垂体-肾上腺轴
压力可促进癫痫的诱发,癫痫患者糖皮质激素水平较高。
下丘脑-垂体-肾上腺轴(HPA轴)是应激反应的核心,包括促肾上腺皮质激素释放因子、促肾上腺皮质激素的分泌以及随后糖皮质激素和儿茶酚胺下游途径的释放。
不同的激素可能有不同的作用:例如,大多数脱氧皮质酮是抗惊厥药,而促肾上腺皮质激素释放激素和皮质酮可诱发癫痫发作。
√肠道微生物调节HPA轴影响癫痫
尽管HPA轴和肠道微生物群之间存在相关性,但具体机制尚未阐明。慢性压力可能会上调糖皮质激素,从而增强谷氨酸信号传导并诱发癫痫发作。肠道微生物群可以通过改变循环细胞因子水平或其他途径影响下丘脑的功能,从而调节HPA轴。
小鼠的应激反应表明,肠道微生物群调节应激依赖性垂体和肾上腺激活,并改变结肠中调节促肾上腺皮质激素释放激素途径的基因表达。慢性压力可能通过肠道微生物群影响HPA轴并促进癫痫。
注:HPA轴、肠道微生物群和癫痫之间的具体关系仍需进一步研究。
Part4
癫痫的代谢标志物
健康人和不同类型癫痫患者之间的肠道微生物及其代谢物差异使其成为癫痫鉴别诊断、预后和治疗监测的潜在代谢标志物。
这里将讨论一些涉及癫痫或是神经活性的物质。
1
短链脂肪酸
使用啮齿动物模型的实验研究检验了短链脂肪酸对宿主神经系统的调节作用。短链脂肪酸调节多种受体,包括普遍存在的多效性G蛋白偶联受体,不仅存在于肠上皮细胞上,而且还存在于脑组织中。
▷调节G蛋白偶联受体影响神经系统
G蛋白偶联受体参与激活抑制性调节性T细胞、辅助性T细胞1和辅助性T细胞17,增强FOXP3转录因子的基因表达并下调促炎细胞因子,例如IL-12,肿瘤坏死因子和核因子-κB(NF-κB)。
短链脂肪酸还能够通过将乙酸盐转化为细胞营养和能量代谢所需的乙酰辅酶A来激活整合mTOR途径。
▷调节组蛋白去乙酰酶影响癫痫
此外,乙酸盐、丙酸盐和丁酸盐可能通过抑制组蛋白去乙酰酶 (HDAC) 或触发乙酰化来引起表观遗传修饰。
组蛋白去乙酰酶已被证明参与神经发生、突触传递、可塑性、脑源性神经营养因子水平的调节、神经胶质细胞发育、与学习和记忆相关的高级脑功能以及抑郁症和精神分裂症等神经系统疾病。
最近的研究已经证实了组蛋白乙酰化在失神性癫痫啮齿动物模型中癫痫发生和相关精神疾病中的作用。在这项研究中,在早期长期给予丁酸盐和丙戊酸(单独或联合)后,大鼠表现出致癫痫活动的数量和持续时间显著减少。
此外,组蛋白乙酰化的增强可以改善抑郁样行为和记忆表现等症状。这些发现强调了组蛋白去乙酰酶抑制剂作为癫痫治疗新策略的能力。
▷促进血清素和儿茶酚胺的合成
短链脂肪酸还可以促进色氨酸羟化酶1和酪氨酸羟化酶基因的转录,从而分别促进肠道血清素和血清儿茶酚胺(即多巴胺、去甲肾上腺素和肾上腺素)的生物合成,这些血清素具有通过自主受体调节中枢神经系统的关键作用。
小鼠下丘脑的谷氨酸和γ-氨基丁酸水平在暴露于醋酸盐或鼠李糖乳杆菌和长双歧杆菌的特定菌株后会发生变化,表现出抑郁和焦虑样表型的减弱。
综上所述,短链脂肪酸作为癫痫的生物标志物,通过影响神经信号传导、血脑屏障和免疫系统等多个途径参与癫痫的发病机制。
2
胆汁酸
胆汁酸是胆汁的主要有机成分,可作为胆固醇、胆红素和异生物质的生物洗涤剂。
胆酸和鹅去氧胆酸是肝脏产生的初级胆汁酸,一旦进入肠道,肠道微生物群就会通过脱羟基作用将胆汁酸转化为次级胆汁酸,包括脱氧胆酸和石胆酸。
在小鼠中,已证明次级胆汁酸是法尼醇X受体的内源性配体,法尼醇X受体是调节肝脂肪生成、胰岛素敏感性和葡萄糖稳态的重要传感器。法尼醇X受体的激活还可以通过增加抗菌基因的表达和阻止细菌易位来抑制肠道微生物的过度生长。
法尼醇X受体在肝脏、肠和皮质神经元中表达。在中枢神经系统中,法尼醇X受体影响γ-氨基丁酸、去甲肾上腺素和血清素的神经传递。
▷胆汁酸与癫痫的炎症程度和发作频率有关
一些研究发现,癫痫患者的胆汁酸代谢存在异常。具体来说,癫痫患者的胆汁酸合成和转运过程可能受到影响,导致胆汁酸浓度的改变。
此外,胆汁酸与肠道微生物群之间存在相互作用,微生物群可以通过代谢胆汁酸来影响其浓度和代谢途径。
一项发表于2020年的研究发现,癫痫患者的血液和脑脊液中的胆汁酸水平明显降低。此外,胆汁酸的降低与癫痫的严重程度和发作频率呈负相关。
这些发现表明,胆汁酸可能在癫痫的发生和发展中发挥一定的作用。
需要指出的是,胆汁酸作为癫痫标志物的研究仍处于初步阶段,尚需进一步的研究来验证这些发现,并深入探索其在癫痫发病机制中的具体作用。
了解胆汁酸与癫痫之间的关系有助于我们更好地理解癫痫的病理生理过程,并为癫痫的预防和治疗提供新的思路。
3
色氨酸及其代谢物
色氨酸是一种重要的氨基酸,它在人体内起着多种生物学功能。它是各种激素、维生素、某些脑神经递质以及抗菌活性所需蛋白质的前体。最近的研究表明,色氨酸代谢异常可能与癫痫有关。
▷色氨酸及其代谢物参与抗癫痫作用
一项对16名难治性癫痫儿童进行的研究表明,色氨酸代谢物可能参与抗癫痫作用。
马吲哚胺2,3-双加氧酶1的激活(分解谷氨酸代谢物)通过改变犬尿氨酸/谷氨酸比例与慢性颞叶癫痫大鼠模型中的抑郁样行为直接相关。
另一项在两种癫痫小鼠模型中进行的重要研究指出,α-乳清蛋白通过提高血浆和大脑中色氨酸的浓度来发挥抗惊厥活性,从而通过微生物群和血清素能受体改善神经传递。
在不同的啮齿动物模型中长期使用α-乳清蛋白治疗可以保护或抑制癫痫发作。
此外,据推测,色氨酸代谢物可作为N-甲基-D-天冬氨酸受体的拮抗剂,从而抑制兴奋性途径。
Part5
肠道微生物群导向的癫痫治疗策略
肠道微生物群的调节可能是癫痫的潜在治疗方法。一方面,调节肠道微生物群可以通过调整与癫痫相关的机制来减少癫痫的发作。
另一方面,药物可以通过直接或间接的方式被肠道微生物群转化为代谢物。对于癫痫患者来说,调整肠道微生物组的组成可能会促进药物代谢和吸收,提高抗癫痫药物的反应性。
肠道微生物群在癫痫中的假设机制和作用

Iannone LF,et al.Neurobiol Dis.2022
在本节中,谷禾将阐述一些基于肠道微生物群的癫痫潜在疗法。如生酮饮食,施用抗生素、益生菌、益生元以及抗癫痫药物和粪便移植对癫痫的影响。

Ding M,et al.Front Immunol.2021
▼
生酮饮食
饮食,尤其是生酮饮食,可以通过塑造肠道微生物群来调节癫痫的发生,生酮饮食是一种高脂肪、低碳水化合物和充足蛋白质的饮食,自1921年以来一直用于治疗难治性癫痫患者。
注:生酮饮食对其他神经系统疾病也有积极作用,如多发性硬化症、帕金森病、阿尔茨海默病和偏头痛。
关于癫痫发作频率,在生酮饮食治疗期间,10%的患者没有癫痫发作,40%的患者癫痫发作频率降低至50%。
生酮饮食对癫痫发作活动的可能影响
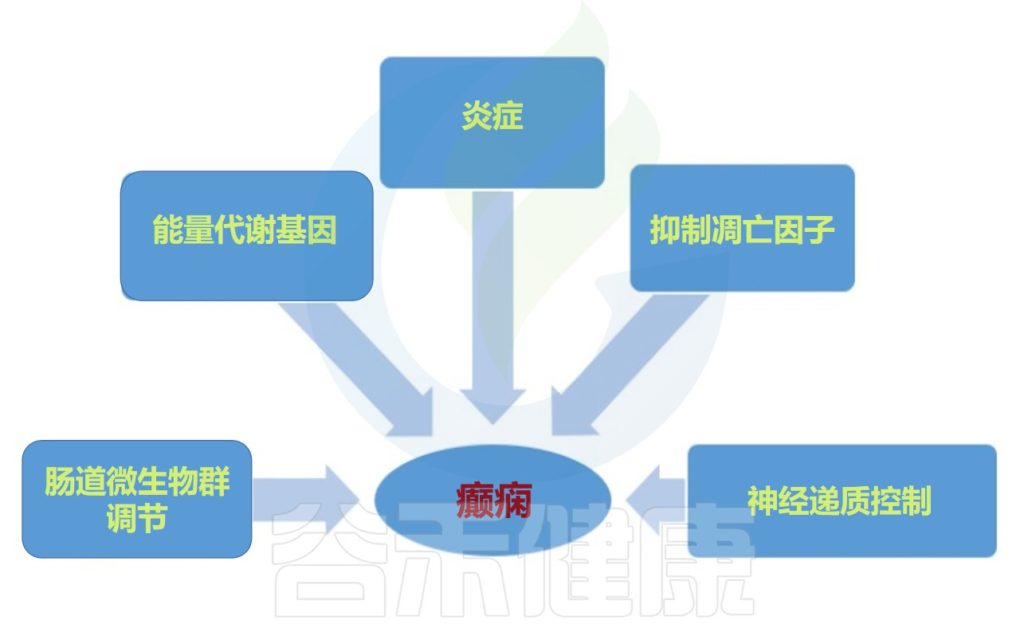
Ułamek-Kozioł M,et al.Nutrients.2019
生酮饮食中脂肪与蛋白质和碳水化合物的经典比例为4:1,这会引发代谢模式从葡萄糖代谢转向脂肪酸代谢。
经典的生酮饮食可以通过多种途径缓解癫痫,包括调节神经递质、脑能量代谢、氧化应激、离子通道和肠道菌群。
•不饱和脂肪酸具有抗癫痫作用
在生酮饮食中,饱和脂肪一直是主要使用的脂肪;然而,动物和人类研究已经证明多不饱和脂肪酸,尤其是Omega-3脂肪酸具有抗癫痫作用。
膳食Omega-3存在于亚麻籽、坚果、深海鱼和海洋哺乳动物中。 Omega-6主要来源于动物产品和植物油,构成现代西方饮食中多不饱和脂肪酸的大部分。
二十二碳六烯酸是大脑中主要的多不饱和脂肪酸,通过多种途径参与神经功能的调节,例如与离子通道的相互作用和神经递质的释放。一项病例对照研究表明,癫痫儿童血清Omega 3/Omega 6 比率低于健康儿童。
体外和体内研究都表明,富含Omega 3脂肪酸的饮食有利于癫痫控制,2021年七项临床试验研究的荟萃分析表明,补充Omega-3可显著降低癫痫发作频率,并且对成人比儿童更有效。
•肠道菌群对生酮饮食抗癫痫治疗具有促进效果
一些临床和实验研究探讨了肠道微生物群对生酮饮食抗癫痫疗法的作用。
通过使用 16S rRNA 测序方法,分析了接受生酮饮食治疗一周的中国儿童耐药性癫痫患者的分类肠道微生物群变化。
生酮饮食调节了不同肠道微生物群的相对丰度
结果表明,生酮饮食增加了特定门的相对表达,包括拟杆菌门和普雷沃氏菌门,同时降低了克罗诺杆菌属、丹毒杆菌属、链球菌属、另枝菌属(Alistipes)、瘤胃梭菌属(Ruminiclostridium)、Barnesiella和肠球菌属的相对表达。
研究人员将这些改变与癫痫发作减少联系起来,因为21%的患者没有癫痫发作,43%的患者癫痫发作减少了 50%。
这些结果得到了后续临床研究的证实。检查了接受生酮饮食治疗的中国儿童耐药性癫痫患者的粪便样本。发现经过六个月的生酮饮食治疗后,β多样性与基线水平有所不同。生酮饮食后,拟杆菌门的相对丰度增加,厚壁菌门和放线菌的比例显著降低。
有趣的是,在对生酮饮食反应较少的剩余50%患者中,梭状芽胞杆菌、瘤胃球菌科、毛螺菌科、另枝菌属和文肯菌科(Rikenellaceae)的相对丰度较高。
这些研究虽然规模较小,但却强化了这样一个假设:通过生酮饮食调节肠道微生物群可以对癫痫患者发挥治疗作用。
生酮饮食对癫痫的影响

Mejía-Granados DM,et al.Seizure.2021
最近的一项研究表明,高脂肪:碳水化合物+蛋白质比例对于癫痫的治疗并不是必不可少的。低脂肪:蛋白质+碳水化合物比例的新组合饮食,包括中链甘油三酯、多不饱和脂肪酸、低血糖指数碳水化合物和高支链氨基酸/芳香族氨基酸比例,也可减少兴奋性驱动并防止啮齿动物模型中的癫痫发作。
饮食干预是控制癫痫有效且有前景的方法,特别是生酮饮食。对微生物群-肠-脑轴的进一步研究将有助于开发更有效的饮食疗法。
▼
微生物群与抗癫痫药物
•肠道微生物群影响抗癫痫药物的功效和毒性
肠道微生物含有丰富的药物代谢酶,可能会影响其药理学,导致药物功效和毒性存在人群差异。
例如,氯硝西泮是一种抗惊厥和抗焦虑药物,被肠道微生物群还原和代谢,导致药物毒性。
•抗癫痫药物会改变微生物群组成
非抗生素药物会在一定程度上改变肠道微生物群。在一项涉及1197种非抗生素药物对肠道微生物群影响的大型研究中,24%的人类靶点药物在体外抑制了菌株的生长。
抗癫痫药物,如卡马西平、丙戊酸和拉莫三嗪影响肠道微生物群组成。小鼠怀孕期间丙戊酸治疗导致粪便微生物群改变,厚壁菌门增加,拟杆菌门减少,这可能与后代的自闭症谱系障碍行为有关。而拉莫三嗪可能通过抑制细菌核糖体生物合成来减少大肠杆菌的生长。
抗癫痫药物或生酮饮食治疗的患者肠道微生物群变化

Amlerova J,et al.Int J Mol Sci.2021
进一步研究抗癫痫药物与肠道微生物的关系,将有助于开发基于肠道微生物调控原理的新型抗癫痫药物。调整肠道微生物成分可以改变抗癫痫药物的代谢过程,从而提高其疗效并减少副作用。
▼
施用抗生素
由于肠道微生物组似乎在包括癫痫在内的几种神经病理性疾病中发生了改变,使用广谱抗生素已成为恢复肠道微生物群生态的可行替代方案,在病理生理学方面显示出有益的结果。
•抗生素治疗可以阻止部分患者的癫痫发作
一些报告表明,抗生素治疗,可能有助于阻止癫痫患者和动物模型的癫痫发作。
用地塞米松(4毫克/天)和米诺环素(50毫克/天)治疗一名患有星形细胞瘤的53岁耐药性癫痫患者,使患者在长达2个月的时间里没有癫痫发作。当地塞米松或米诺环素治疗停止时,癫痫发作频率突然增加至每周7次癫痫发作。
对六名接受抗生素治疗的难治性癫痫患者的回顾性研究表明,某些抗生素可以在短期内减少癫痫发作的频率。
抗生素治疗对癫痫的影响

Mejía-Granados DM,et al.Seizure.2021
•部分抗生素可能也会诱发癫痫
抗生素可能通过干扰肠道菌群和肠-脑轴来诱导癫痫发作或降低癫痫发作频率。然而,某些抗生素也会诱发癫痫:例如,内酰胺类抗生素,包括青霉素、头孢菌素和碳青霉烯类,最有可能引起癫痫发作。
一些青霉素如第四代头孢菌素、亚胺培南和环丙沙星,可能会导致症状性癫痫发作的风险增加。
因此,在这些患者中使用抗生素时应密切监测血清水平和脑电图。未来还需要进一步研究明确各种抗生素对癫痫的具体作用和机制。
▼
补充益生菌
最近研究了补充益生菌在癫痫发作和癫痫中的效果。一项临床试验中,由43名西班牙耐药性癫痫患者组成的队列接受了益生菌补充剂的治疗。
益生菌补充剂包括每日两剂乳杆菌(嗜酸乳杆菌、植物乳杆菌、干酪乳杆菌、瑞士乳杆菌、短乳杆菌和乳杆菌)、乳双歧杆菌和唾液链球菌,持续4个月。
•补充益生菌降低了部分癫痫患者的发作频率
研究报告称,补充益生菌可使28.9%的患者癫痫发作频率减少高达50%。其中76.9%的改善患者在停药4个月后仍保持较低的癫痫发作频率。然而,48.9%的患者对补充益生菌没有反应。
此外,益生菌反应组的生活质量得分显著改善。有趣的是,补充益生菌似乎可以使γ-氨基丁酸血清水平升高和白细胞介素-6水平降低。
•益生菌还可以减轻癫痫发作的严重程度
在戊四氮诱导的化学点燃小鼠模型中,益生菌补充组没有表现出完全点燃,并且小鼠脑组织中的γ-氨基丁酸增加,这表明补充益生菌可以显著降低癫痫发作的严重程度。
化学性点燃是用亚惊厥剂量的兴奋剂连续间隔投药逐渐诱发癫痫发作。
在治疗戊四氮诱导的小鼠癫痫发作时与生酮饮食、合生元或发酵乳杆菌(Lactobacillus fermentum MSK 408) 合用可以减少生酮饮食的副作用,而不影响其抗癫痫作用。
生酮饮食和Lactobacillus fermentum MSK 408均通过调节肠道微生物群来增加γ-氨基丁酸代谢。
补充益生菌对癫痫的影响

Mejía-Granados DM,et al.Seizure.2021
这些研究是补充益生菌治疗难治性癫痫的初步观察,还需要在更大规模的安慰剂对照试验和更严格的动物实验中进行进一步的理论验证和机制探索。
益生菌有潜力成为难治性癫痫的补充治疗,并可与生酮饮食疗法联合使用以减少副作用。
扩展阅读:如何调节肠道菌群?常见天然物质、益生菌、益生元的介绍
▼
粪菌移植
粪便微生物群移植包括将健康捐赠者的粪便微生物群溶液注入接受者的肠道中,以恢复正常的肠道微生物群落。
粪菌移植已广泛应用于多种神经系统疾病,包括阿尔茨海默病、帕金森病、自闭症、多发性硬化症和癫痫,对这些疾病均显示出有益的作用。
•粪菌移植后癫痫发作频率和症状缓解
一些研究评估了粪菌移植对癫痫患者和动物模型的影响。对一名患有慢性病和癫痫的17岁女孩进行3次粪菌移植治疗后,癫痫发作频率得到了有益的影响。粪菌移植20个月后,患者癫痫发作完全缓解,不再需要抗癫痫药物。
此外,衡量这种疾病严重程度的疾病活动指数也从361点显著下降至131点。粪菌移植治疗前(约70天)失调的月经周期在粪菌移植治疗后(约30天)也得到恢复。
粪菌移植对癫痫的影响

编辑
Mejía-Granados DM,et al.Seizure.2021
扩展阅读:粪菌移植——一种治疗人体疾病的新型疗法
注意
尽管有证据表明健康的粪菌移植对癫痫有益,但仍有一些问题需要在进一步的研究中解决。例如,粪菌移植发挥其抗癫痫作用的机制、其有益作用的持久性以及参与此类结果的细菌属或门。
此外,粪菌移植可能会破坏基线微生物群多样性,导致对多种有害微生物的定植抵抗力崩溃。因此,在大规模临床应用之前,还需要更长期的随访研究来确定粪菌移植对癫痫患者的有效性和安全性。
结语
随着研究的深入,肠道微生物群与癫痫之间千丝万缕的联系逐渐被揭示,人们对它们的功能有了更深入的了解。
目前,一些临床研究已证实难治性癫痫患者、药物敏感患者和健康对照者的肠道菌群存在差异。同时,肠道菌群还在癫痫的治疗中影响生酮饮食、抗癫痫药物等的治疗效果。
总体而言,未来微生物组特异性治疗可能是治疗癫痫的有效选择。发现肠道微生物群和癫痫之间的关系将有助于我们更好地了解癫痫的发病机制,从而提高癫痫患者的生活质量。
相关阅读:
中医药治疗抑郁症——来自肠道菌群的解释
肠道微生物组在人类神经系统疾病中的作用
肠道微生物群在多发性硬化中的作用
饮食与抑郁症密不可分,一文涵盖多种生物学机制
一文了解渐冻症发病机理及相关干预措施
环境污染物通过肠脑轴影响心理健康,精神益生菌或将发挥重要作用
肠道微生物与帕金森以及相关影响因素
阿尔茨海默病de饮食-微生物-脑轴
主要参考文献
Wang Y, Zhuo Z, Wang H. Epilepsy, gut microbiota, and circadian rhythm. Front Neurol. 2023 May 18;14:1157358.
Iannone LF, Gómez-Eguílaz M, De Caro C. Gut microbiota manipulation as an epilepsy treatment. Neurobiol Dis. 2022 Nov;174:105897.
Liu T, Jia F, Guo Y, Wang Q, Zhang X, Chang F, Xie Y. Altered intestinal microbiota composition with epilepsy and concomitant diarrhea and potential indicator biomarkers in infants. Front Microbiol. 2023 Jan 11;13:1081591.
Zeng Y, Cao S, Yang H. Roles of gut microbiome in epilepsy risk: A Mendelian randomization study. Front Microbiol. 2023 Feb 27;14:1115014.
Ułamek-Kozioł M, Czuczwar SJ, Januszewski S, Pluta R. Ketogenic Diet and Epilepsy. Nutrients. 2019 Oct 18;11(10):2510.
Dahlin M, Prast-Nielsen S. The gut microbiome and epilepsy. EBioMedicine. 2019 Jun;44:741-746.
Mejía-Granados DM, Villasana-Salazar B, Lozano-García L, Cavalheiro EA, Striano P. Gut-microbiota-directed strategies to treat epilepsy: clinical and experimental evidence. Seizure. 2021 Aug;90:80-92.
Ding M, Lang Y, Shu H, Shao J, Cui L. Microbiota-Gut-Brain Axis and Epilepsy: A Review on Mechanisms and Potential Therapeutics. Front Immunol. 2021 Oct 11;12:742449.