今天给同学们分享一篇生信文章“Exploring the Pathogenesis of Psoriasis Complicated With Atherosclerosis via Microarray Data Analysis”,这篇文章发表在Front Immunol期刊上,影响因子为7.3。

结果解读:
差异表达基因的鉴定
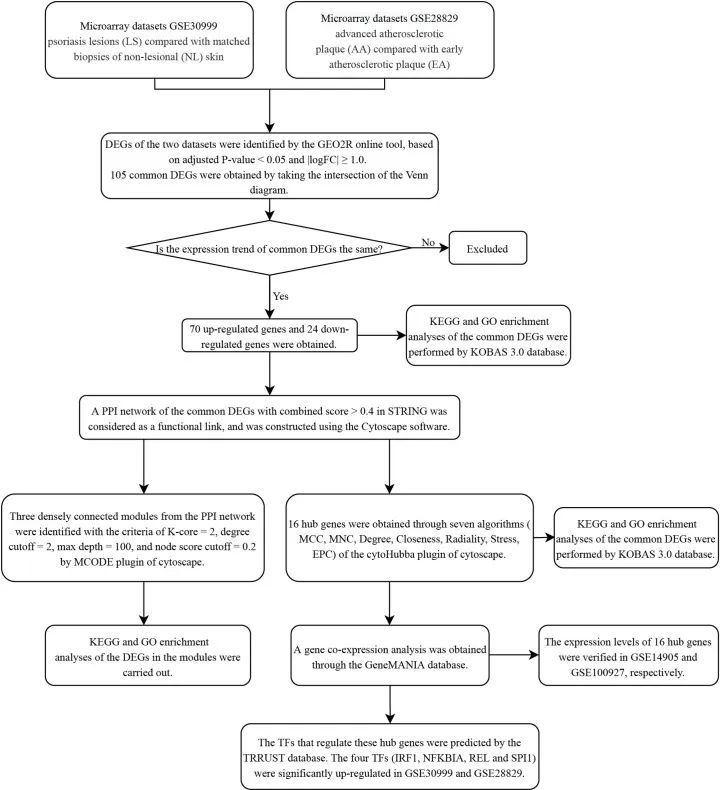
该研究的研究流程图如图1所示。在标准化微阵列结果后,鉴定出差异表达基因(GSE30999中的3318个和GSE28829中的338个)(图2A、B)。在维恩图的交集中,获得了105个共同的差异表达基因(图2C)。随后,在排除了在GSE30999和GSE28829中表达趋势相反的基因后,获得了94个差异表达基因。
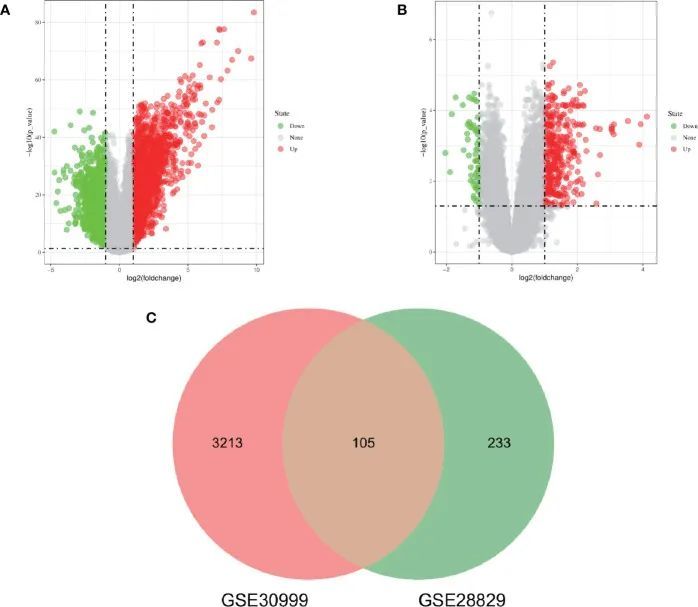
常见差异表达基因(DEGs)功能特征分析
为了分析涉及94个常见差异表达基因(DEGs)的生物功能和通路,进行了GO和KEGG通路富集分析。GO分析结果显示,这些基因主要富集在蛋白质结合(P = 7.11E-15)、中性粒细胞颗粒溶解(P = 5.81E-10)、免疫应答(P = 1.55E-07)、趋化作用(P = 3.91E-06)和细胞因子介导的信号通路(P = 5.19E-06)(图3B)。在KEGG通路方面,三个显著富集的通路是趋化因子信号通路(P = 7.44E-05)、细胞因子-细胞因子受体相互作用(P = 4.68E-04)和白细胞经内皮迁移(P = 4.68E-04)(图3C)。这些结果强烈表明趋化因子和细胞因子共同参与了这两种炎症性疾病的发生和发展。
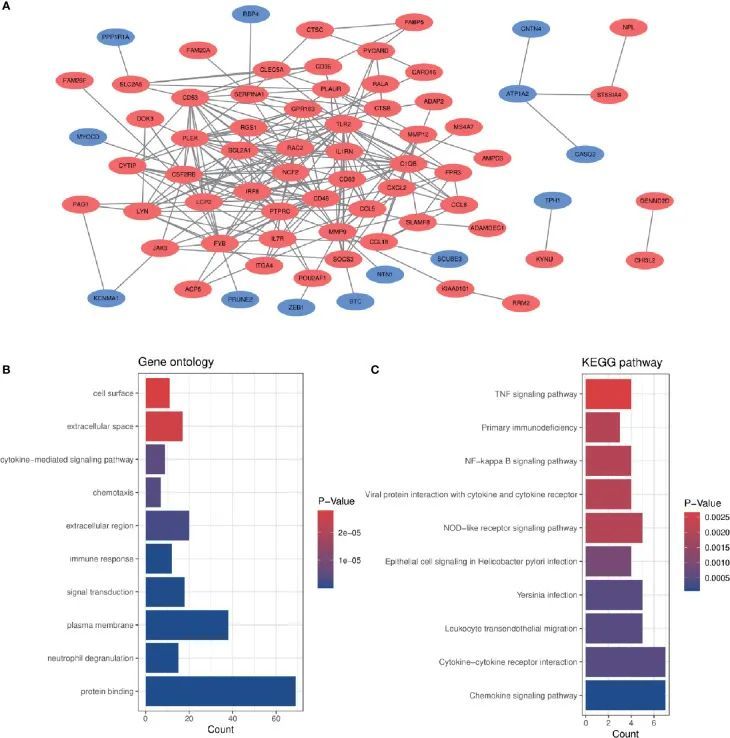
PPI网络构建和模块分析
使用Cytoscape构建了具有综合得分大于0.4的常见差异表达基因(DEGs)的PPI网络,其中包含72个节点和230个相互作用对(图3A)。通过Cytoscape的MCODE插件获得了三个紧密连接的基因模块,包括24个常见DEGs和59个相互作用对(图4A-C)。GO分析显示这些基因与炎症和免疫反应相关(图4D)。KEGG通路分析显示它们主要参与TNF信号通路、细胞因子-细胞因子受体相互作用和白细胞经内皮迁移(图4E)。
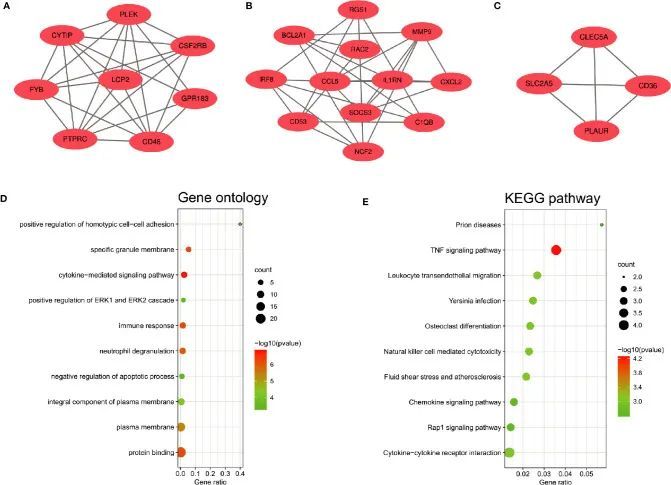
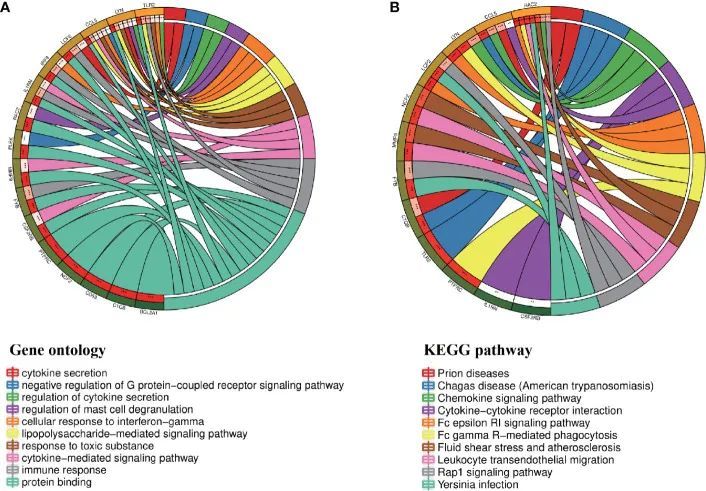
选择和分析关键基因
通过插件cytoHubba的七个算法,作者计算出了前20个关键基因。在Venn图的交集中,作者发现了16个共同的关键基因,包括LYN、CSF2RB、IL1RN、RAC2、CCL5、IRF8、C1QB、MMP9、PLEK、PTPRC、FYB、BCL2A1、LCP2、CD53、NCF2和TLR2(图5A)。表2显示了它们的全名和相关功能。基于GeneMANIA数据库,作者分析了这些基因的共表达网络和相关功能。这些基因显示出复杂的蛋白质相互作用网络,其中包括80.18%的共表达、11.58%的物理相互作用、4.81%的共定位、2.45%的预测和0.99%的通路(图5B)。GO分析显示,这些基因主要参与蛋白质结合、脂多糖介导的信号通路、免疫应答、细胞因子介导的信号通路和对干扰素-γ的细胞反应(图6A)。这些结果强调了脂多糖和细胞因子在这两种疾病中的重要作用。此外,KEGG通路分析显示它们主要参与FcεRI信号通路、FcγR介导的吞噬作用、白细胞经内皮细胞迁移和趋化因子信号通路。有趣的是,三个基因(NCF2、RAC2和MMP9)还参与了流体剪切应力和动脉粥样硬化(图6B)。
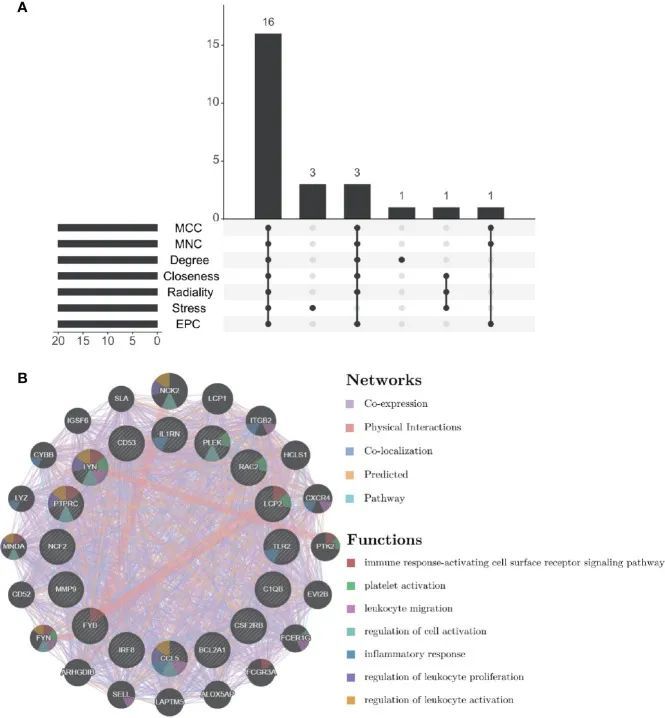
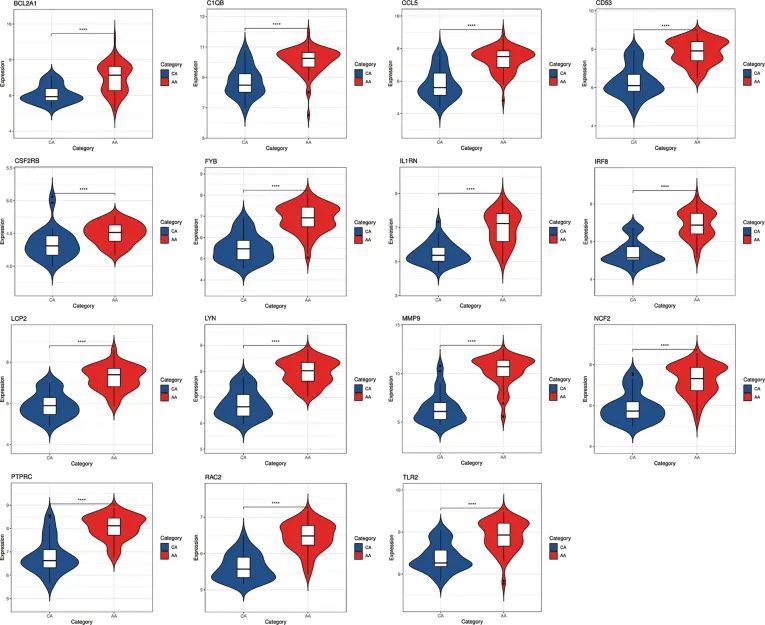
验证关键基因表达
为了验证这些关键基因表达水平的可靠性,作者选择了另外两个包含银屑病损和动脉粥样硬化斑块的数据集,并分析了这些关键基因的表达水平。结果显示,与正常皮肤和皮损旁正常组织相比,所有关键基因在银屑病皮损中均显著上调(图7)。同样,在动脉粥样硬化斑块中,所有基因的表达水平(GSE100927中PLEK的表达值缺失)也高于正常血管组织(图8)。

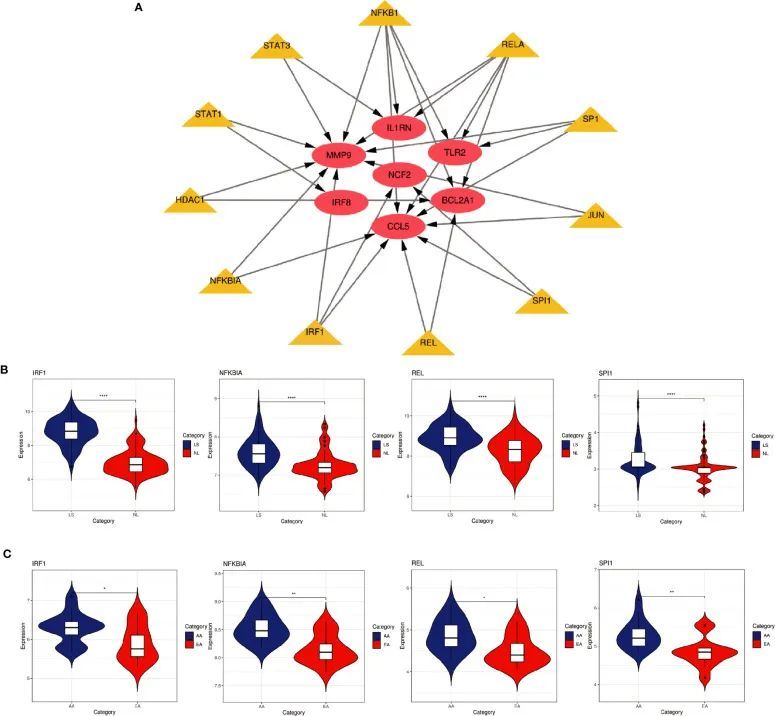
预测和验证转录因子
根据TRRUST数据库,作者发现有11个转录因子可能调控这些基因的表达(图9A)。进一步验证,作者发现有四个转录因子在银屑病病变和动脉粥样硬化斑块中高度表达(图9B,C)。它们共同参与了四个关键基因(CCL5,NCF2,MMP9和BCL2A1)的调控。
总结
总之,作者确定了银屑病和动脉粥样硬化的常见DEG,并进行了富集和PPI网络分析。作者发现银屑病和动脉粥样硬化有许多共同的致病机制,这些机制可能是由特定的中枢基因介导的。本研究为进一步研究银屑病并发动脉粥样硬化的分子机制提供了新的见解。

![[MySQL] SQL优化之性能分析](https://img-blog.csdnimg.cn/direct/3fbe5fe455e24a7fb4fd491ca3752b33.png)