ctDNA检测方便快捷、安全性好、可反复取样,在CRC精准治疗领域具有广阔的应用前景。动态ctDNA检测有望指导患者抗EGFR单抗治疗的“再挑战”,为患者带来更多希望。但最佳抗EGFR单抗再挑战策略、对比标准三线治疗的疗效差异及ctDNA检测在其中扮演的角色尚无定论。本期臻知识结合近期发表在JAMA Oncology杂志上的文章进行解读。
对于RAS野生型左半mCRC,抗EGFR单抗联合化疗是一线标准治疗方案,但在治疗过程中,大部分患者会因RAS突变等获得性耐药而导致疾病进展。二线治疗后可因RAS突变清零而恢复抗EGFR单抗治疗的敏感性,EGFR单抗再挑战的概念由此应运而生。但抗EGFR单抗联合曲氟尿苷替匹嘧啶可否进一步改善难治性RAS野生型mCRC预后及最佳优势人群筛选策略尚无定论。今天分享的发表在JAMA Oncology杂志上的VELO研究试图回答以上问题。
该研究为一项II期开放标签、随机对照研究。该研究共纳入62例难治性RAS野生型mCRC患者,所有患者随机分配(1:1)接受单纯曲氟尿苷替匹嘧啶治疗(A组,n=31)或帕尼单抗联合曲氟尿苷替匹嘧啶治疗(B组,n=31)。结果发现联合组中位PFS约4.0个月,而单药组中位PFS仅2.5个月(HR=0.48,P=0.007)。对比单纯化疗,治疗前血浆样本RAS/BRAF野生型患者从抗EGFR单抗再挑战治疗中获益更大,6个月PFS率分别为38.5%和13.0%(p=0.047),12个月PFS率分别为15.4%和0(p=0.052)。再挑战治疗前65.2%患者为KRAS、NRAS、BRAF V600E、EGFR、ERBB2、MAP2K1和PIK3CA基因野生型,这组患者中位PFS可达6.4个月。
综上,本研究证实针对难治性RAS野生型mCRC患者,在标准三线曲氟尿苷替匹嘧啶基础上联合帕尼单抗可将疾病控制率提升1倍左右,且未出现治疗相关死亡或停药事件,显著改善患者PFS。经ctDNA检测确定EGFR信号通路相关基因为野生型的患者PFS更长,提示基于ctDNA的液体活检可助力抗EGFR单抗再挑战优势人群筛选,提高治疗有效率,也期待后续更大型的随机对照研究可对更合理的抗EGFR单抗再挑战模式进行探索,从而改善目前的三线标准治疗方式。
摘要
目前,转移性结直肠癌(mCRC)的三线治疗效果不尽如人意。抗EGFR抑制剂治疗再挑战可能使部分RAS野生型患者获益。本研究对比帕尼单抗联合曲氟尿苷替匹嘧啶与曲氟尿苷替匹嘧啶单药在RAS野生型mCRC患者三线治疗中的疗效。结果发现联合组中位PFS约4.0个月,而单药组中位PFS仅2.5个月(HR=0.48,P=0.007)。对比单纯化疗,治疗前血浆样本RAS/BRAF野生型患者从抗EGFR单抗再挑战治疗中获益更大,6个月PFS率分别为38.5%和13.0%(p=0.047),12个月PFS率分别为15.4%和0(p=0.052)。再挑战治疗前65.2%患者为KRAS、NRAS、BRAF V600E、EGFR、ERBB2、MAP2K1和PIK3CA基因野生型,这组患者中位PFS为6.4个月。本研究初步证实难治性RAS野生型mCRC的三线治疗,帕尼单抗联合曲氟尿苷替匹嘧啶相较于曲氟尿苷替匹嘧啶单药治疗可显著改善患者预后,可根据血浆NGS检测结果指导抗EGFR单抗再挑战。
研究背景
抗EGFR单抗体联合细胞毒药物为RAS野生型mCRC患者的标准治疗方法。尽管初始治疗有效,但不可避免地会因发生KRAS或NRAS等获得性耐药相关突变而导致治疗失败。接受化疗联合西妥昔单抗或帕尼单抗时,多数RAS野生型肿瘤细胞被杀死,但RAS突变型癌细胞的基因选择随着肿瘤进展而发生。后续化疗联合抗血管生成药物可导致RAS突变克隆消失,恢复肿瘤细胞对抗EGFR药物的敏感性。mCRC二线治疗失败后可接受瑞戈非尼或曲氟尿苷替匹嘧啶治疗,但患者PFS及OS获益有限。因此有学者建议二线治疗失败后RAS野生型患者进行抗EGFR单抗再挑战,目前已有3项单臂II期研究支持抗EGFR治疗再挑战。但关于最佳抗EGFR再挑战治疗模式及其与最佳标准治疗的对比尚无定论。研究者开展本项名为VELO的II期开放标签、RCT研究,旨在探索帕尼单抗联合曲氟尿苷替匹嘧啶相较于曲氟尿苷替匹嘧啶单药治疗之间的疗效差异。
研究方法
本研究入组2019年6月至2022年4月来自意大利7家医学中心的难治性RAS野生型mCRC患者。所有患者一线接受化疗联合抗EGFR单抗治疗且实现完全缓解(CR)或部分缓解(PR),并在二线治疗时停用抗EGFR单抗≥4个月。患者以1:1随机分入帕尼单抗联合曲氟尿苷替匹嘧啶治疗组(B组)或单纯曲氟尿苷替匹嘧啶治疗组(A组)。主要研究终点为PFS,次要研究终点包括ORR、不良反应发生率和OS。探索性分析包括血浆样本基线和治疗结束后的NGS基因组分析。所有患者再挑战治疗前均经KRAS、NRAS及BRAF V600E检测。
研究结果
研究共纳入62例患者,入组流程见图1。治疗前液体活检显示,无患者存在BRAF V600E突变,A组74.2%为RAS/BRAF野生型,B组此比例为83.9%。
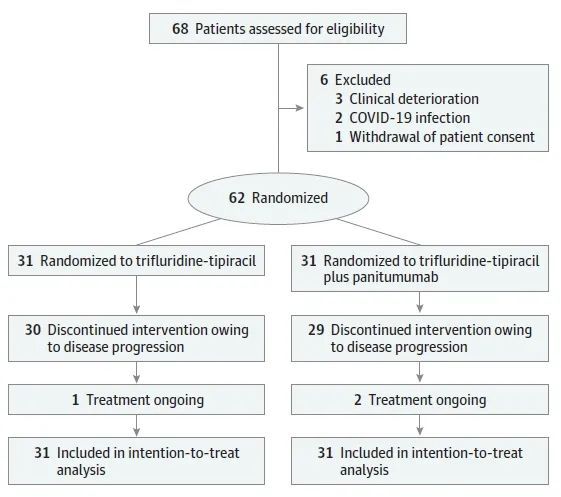
图1. 研究流程
B组和A组中位治疗周期分别为4和2个周期;3-4级不良反应发生率分别为51.6%、29.0%。未出现治疗相关死亡或停药事件。B组和A组分别有51.6%及29.0%患者存在药物减量。
研究达到主要研究终点。帕尼单抗联合曲氟尿苷替匹嘧啶治疗组PFS延长(4.0月vs 2.5月),较单药组减少52%疾病进展风险(图2A)。仅B组出现3例(9.7%)PR患者。B组和A组治疗4月的DCR率分别为74.2%、38.7%。治疗6月、12月的PFS分别为35.5% 和 9.7%(P=0.02)、12.9%和 0%(P=0.04)。
对于治疗前RAS/BRAF ctDNA野生型患者,B组和A组中位PFS分别为4.5月、2.6月(图2B)。DCR率分别为80.7%、47.8%,6个月PFS率分别为38.5%和13.0%(p=0.047),12个月PFS率分别为15.4%和0(p=0.052)。而对于治疗前ctDNA检测提示RAS/BRAF突变型的患者,两组间的PFS不存在显著差异(HR=0.72;95%CI:0.15-1.75,p=0.29)(图2C)。B组中,65.2%患者为KRAS、NRAS、BRAF V600E、EGFR、ERBB2、MAP2K1和PIK3CA野生型(图2D)中位PFS为6.4个月。其中2例患者PR,11例患者SD,仅2例患者出现PD。
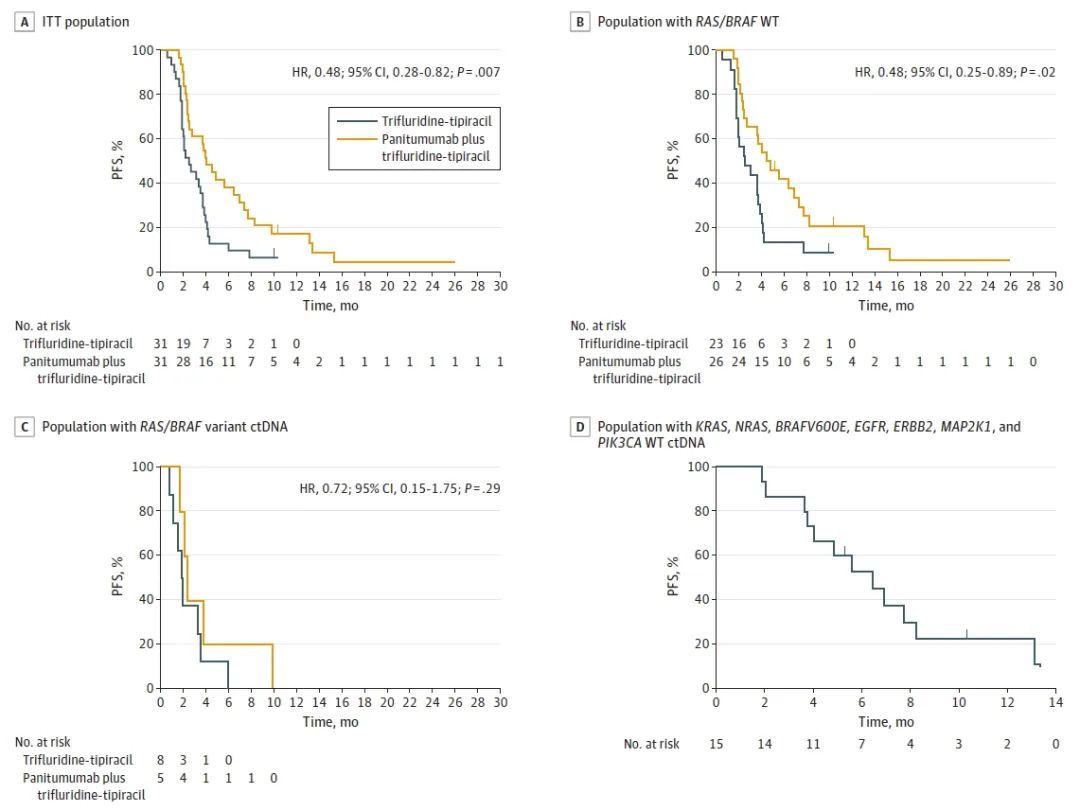
图2. 不同分组患者的PFS生存曲线
讨论
VELO研究为首个评估抗EGFR药物联合标准治疗(曲氟尿苷替匹嘧啶)在RAS野生型mCRC患者中再挑战的II期RCT研究。研究已达到主要研究终点,帕尼单抗联合曲氟尿苷替匹嘧啶治疗组的疾病进展风险降低52%,DCR率几乎为单药组的2倍(74.2% vs 38.7%)。尽管样本量小,但仍为抗EGFR治疗再挑战提供临床依据。
研究同样支持可根据治疗前血浆ctDNA状态进行患者筛选。再挑战前血浆RAS/BRAF阴性患者可从联合组治疗中获益并降低疾病进展风险。基于NGS的血浆ctDNA检测可对适合抗EGFR治疗再挑战患者进行精准选择。针对基线及PD时的血浆样本进行NGS检测,发现帕尼单抗联合曲氟尿苷替匹嘧啶治疗组耐药时多携带EGFR信号通路相关耐药突变。
参考文献:
Panitumumab Plus Trifluridine-Tipiracil as Anti–Epidermal Growth Factor Receptor Rechallenge Therapy for Refractory RAS Wild-Type Metastatic Colorectal Cancer: A Phase 2 Randomized Clinical Trial. JAMA Oncology. 2023 MAY 18.








![[鹏城杯 2022]简单的php - 无数字字母RCE(取反)【*】](https://img-blog.csdnimg.cn/f86d1776abe04b54a02d7d21e9fd56e2.png)