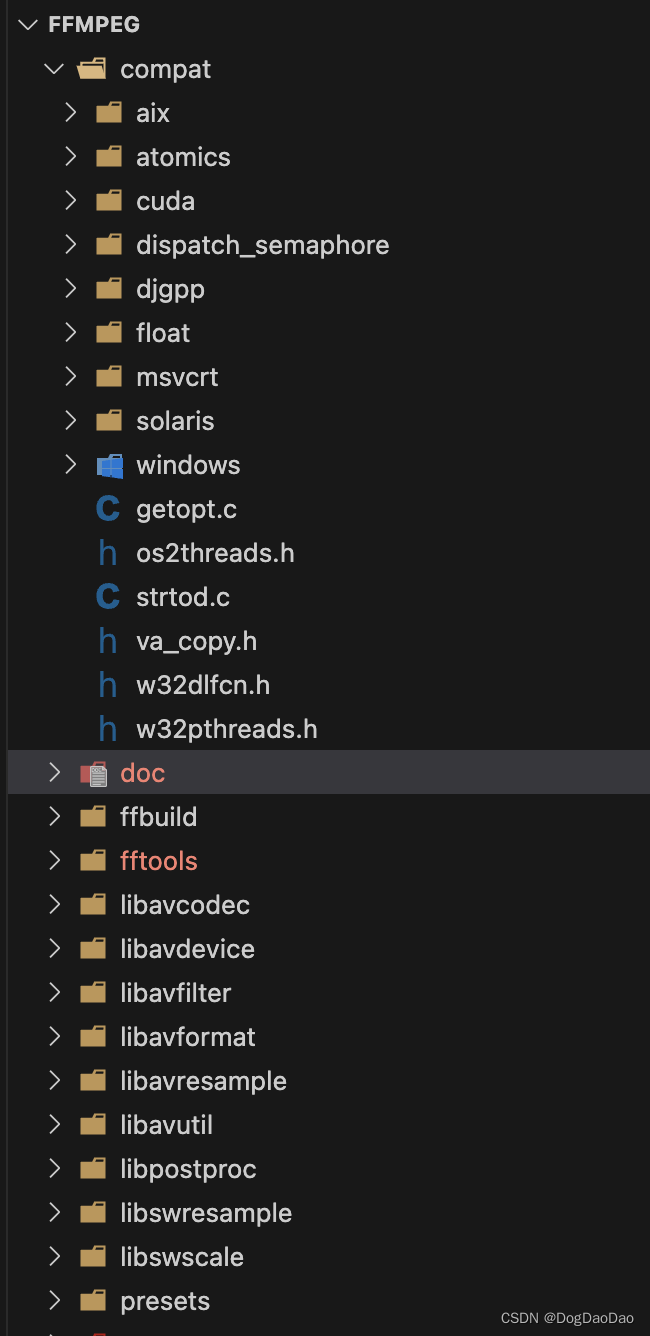
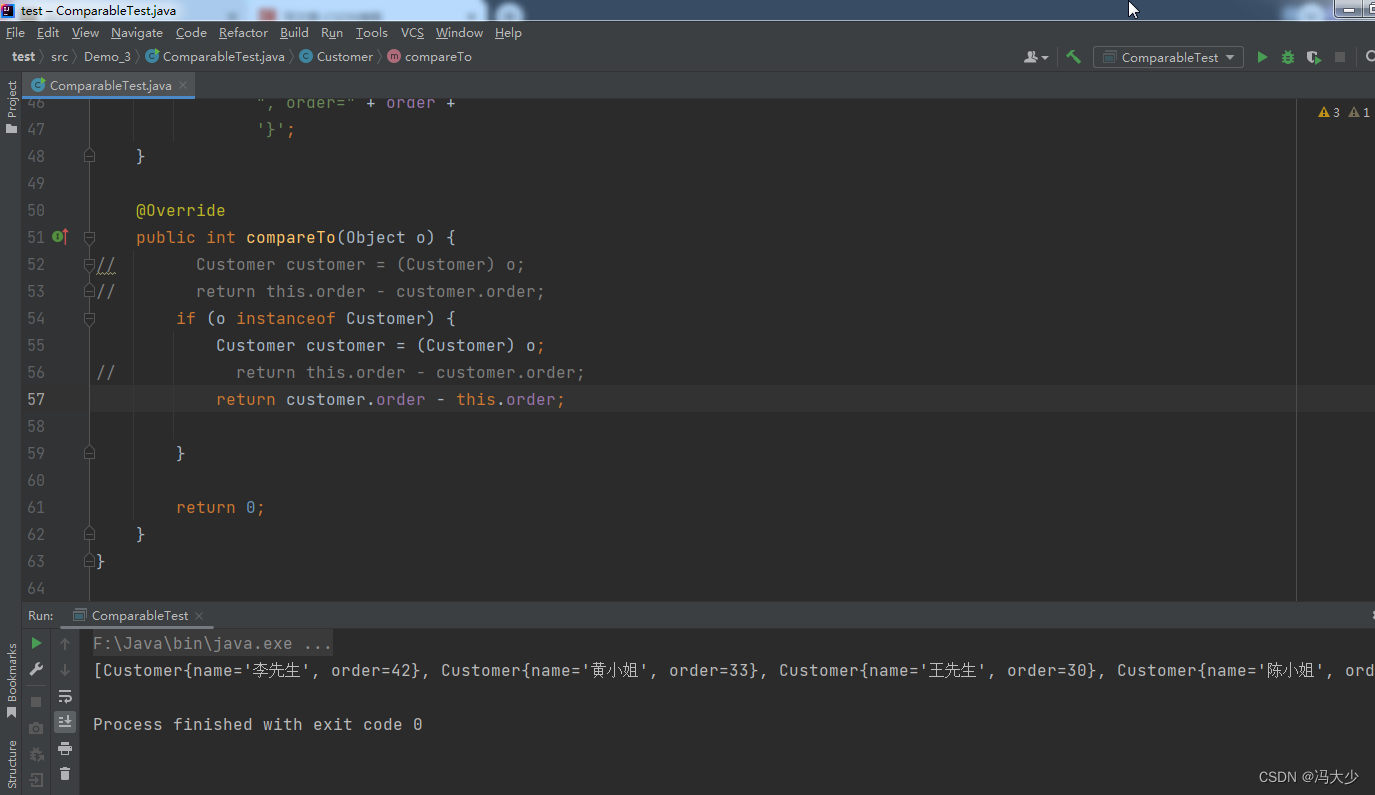
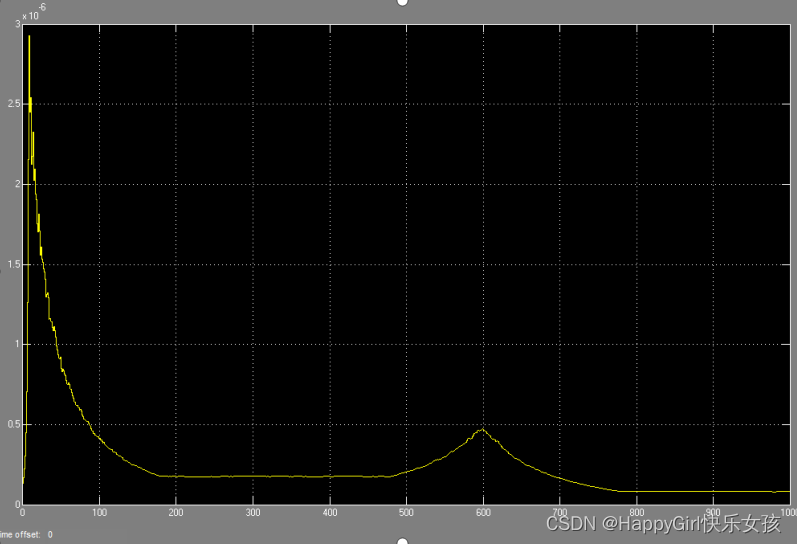
光谱产生的原因:原子中电子在轨道上跃迁产生,如莱曼系为电子从n'=2,3,4等轨道跃迁到n=1的基态轨道产生。
中心的原点为原子核,中心最接接近原子核的圆为n=1的电子轨道。
r_n=a_0n^2,轨道大小正比于n的平方
根据电子轨道图即可以获得光谱图。莱曼图的主线谱线为n'=2跃迁到n=1产生。对应的谱线可以画成n=2->n=1的一条带箭头的线表示。
莱曼系的第二条谱线为n'=3->n=1的一条带箭头的线,依次可以画出整个莱曼系所有谱线构成一个莱曼系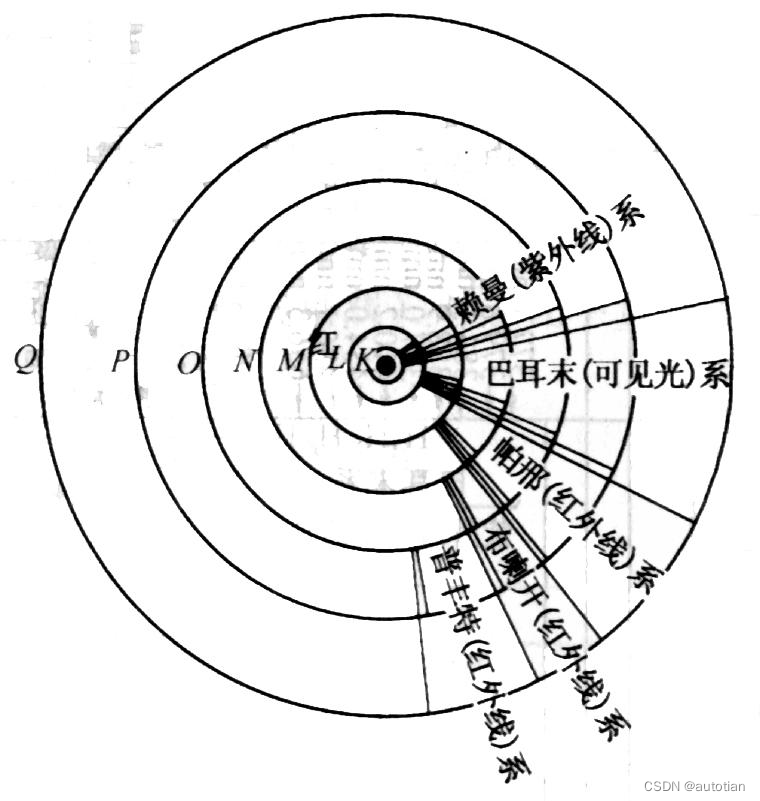
圆形电子轨道表示谱线并不方便,为了更方便的表示电子跃迁和谱线,引入能级图

原子能级图:按照能量大小的比例画出来。
横线表示电子的能级
横线之间的距离表示能级之间的能差
横线两边分别标能量和量子数(n)
谱线是直接在电子初能级和末能级之间画一条带箭头的直线。
谱线方向由初态指向末态。
箭头向下表示辐射出光子,从低能级跃迁到高能级。箭头向上表示要吸收光子。
氢原子的莱曼系就是从高能级往n=1能级跃迁
对于波尔模型而言,当原子吸收外部光子能量(外部能量E)
若外部能量E与原子中两个能级之间的能量差\delta E相等:称之为共振,电子可以吸收能量发生跃迁
能量小于\delta E:电子不会吸收能量发生跃迁。因为两个能级之间没有中间能级,让电子停留。
当能量E高于\delta E:一个光子的能量就是一个hv是不可以再分的,电子吸收这个光子能量,没有能级让电子停留。所以此时,电子也是不吸收光子能量()吸收几率与共振情况非常小,完全可以忽略。
如果外部能量是来自于电子这样的粒子,电子是可以将其一部分的动能传递给原子,剩下的部分自己保留。
所以如果能量来自于电子,电子的动能大于\delta E,同样可以使


![[ 应急响应基础篇 ] evtx提取安全日志 事件查看器提取安全日志](https://img-blog.csdnimg.cn/ce0be5ee41dc4990bfe0536d72683fdb.png)

![[建议收藏]45 个 Git 经典操作场景,专治各种不会合并代码的童鞋~~](https://img-blog.csdnimg.cn/20210818181529121.png?x-oss-process=image/watermark,type_ZmFuZ3poZW5naGVpdGk,shadow_10,text_aHR0cHM6Ly9ibG9nLmNzZG4ubmV0L3FxXzQxNTcwNjU4,size_16,color_FFFFFF,t_70)