国内外上市医疗器械产品数据及注册备案信息是医疗器械行业中极其重要的情报之一。大多数医械人都知道国内医疗器械产品信息可在NPMA及各省市药监局官网查询,但对于国际的医疗器械产品数据披露平台,由于语言壁垒及网页设计习惯差异,查询却不太通畅。
本文将盘点全球各国医疗器械产品数据及注册备案信息官网查询系统,整理医疗器械产品数据库直达入口,减少检索工作,为医械人提供更便捷的信息查询途径。
1.中国:国家药品监督管理局NMPA(医疗器械产品官方查询系统)
国家药品监督管理局NMPA是我国医疗器械及药品的监督管理机构,所有在境内生产、销售及使用的医疗器械产品均受其管辖。国家药监局是医疗器械产品数据查询的权威官方系统,也是每一个医械人必备及常用的网站。
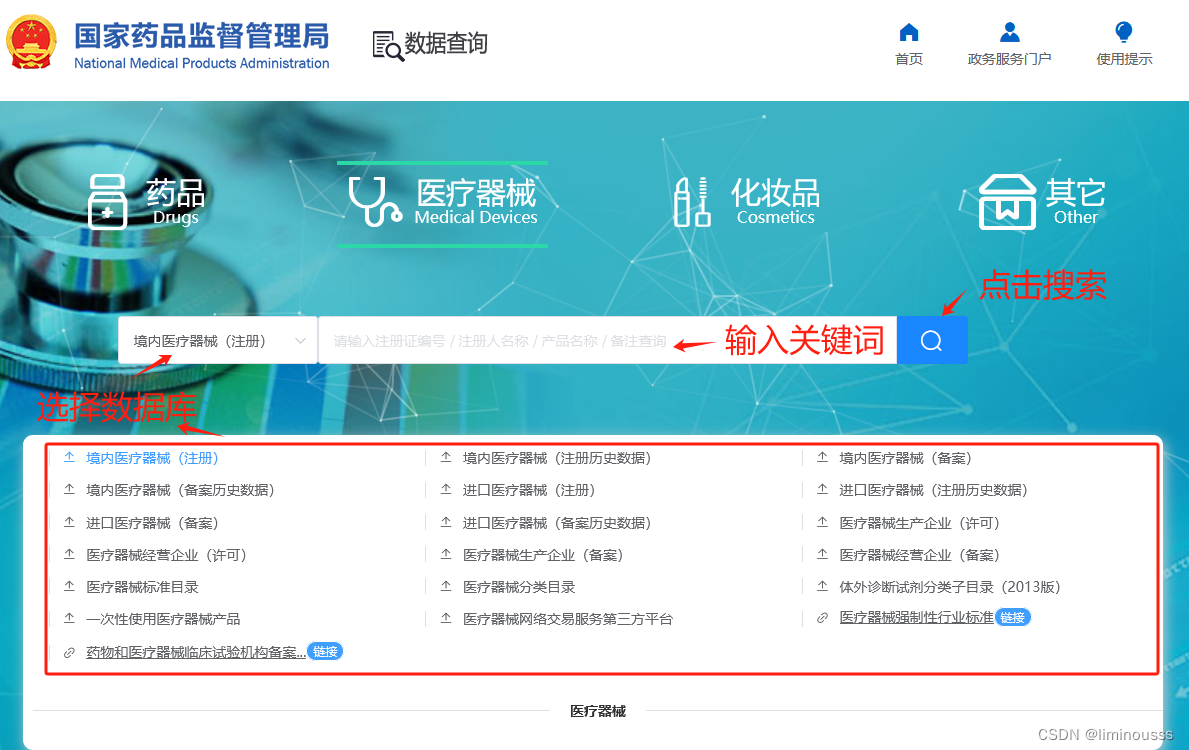
①查询方法:
查询通道:
国家药品监督管理局--->医疗器械--->医疗器械查询---->输入关键词
查询直达链接:https://www.nmpa.gov.cn/datasearch/home-index.html#category=ylqx
②查询范围(数据库):
医疗器械产品相关:境内医疗器械(注册)、境内医疗器械(注册历史数据)、境内医疗器械(备案)、境内医疗器械(备案历史数据)、进口医疗器械(注册)、进口医疗器械(注册历史数据)、进口医疗器械(备案)、进口医疗器械(备案历史数据)
医疗器械企业相关:医疗器械生产企业(许可)、医疗器械经营企业(许可)、医疗器械生产企业(备案)、医疗器械经营企业(备案)、
医疗器械标准相关:医疗器械标准目录、医疗器械分类目录、体外诊断试剂分类子目录(2013版)、一次性使用医疗器械产品、医疗器械网络交易服务第三方平台
③查询技巧:
先选择具体数据库。
选择以上三大类相关数据库中的一个或其中几个(同时选择不能超过3个),注册号中“准”为境内医疗器械,“进”为进口医疗器械,一类医疗器械(注册证号从左往右数第5个数字为1)选择产品备案数据库,二三类(注册证号第5个数字为2或3)医疗器械选择产品注册数据库。
输入关键词,点击搜索。
可选择注册证编号、注册人名称、产品名称等有效信息进行输入检索。只支持在线查看,不支持导出下载。也不支持范围查询、数据分析。
全量数据查询。
若想查看医疗器械产品所有数据总量或列表,可在关键词搜索栏中输入“公司”,便可得到所有医疗器械产品数据。此方法适用于产品及公司数据库。
2.全球:数屿医械(各国医疗器械产品数据查询及分析应用)
行业垂直数据库,集齐了中国、中国香港、中国台湾、美国、欧盟、英国、日本、加拿大、俄罗斯、韩国等20+个主流国家及地区的上市医疗器械产品数据信息,可通过多种方式进行检索,支持数据可视化结果分析及导出。
①查询方法:
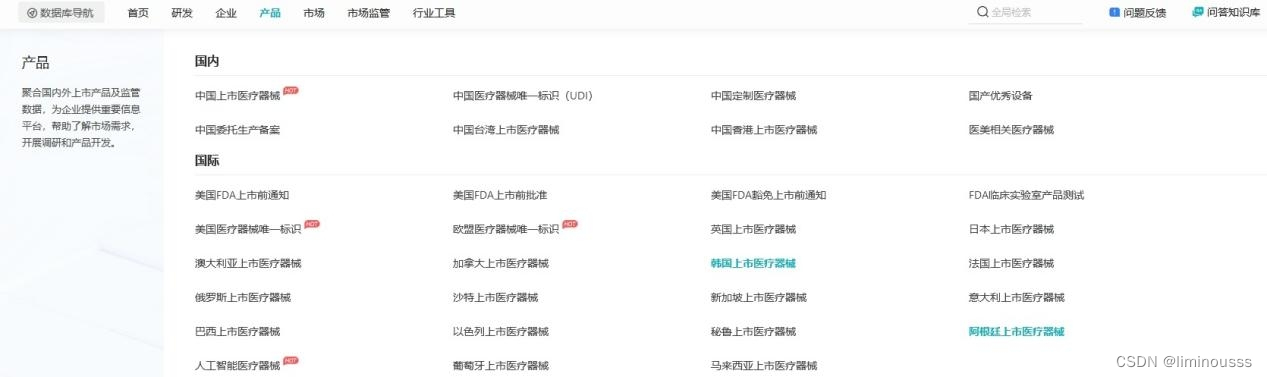
查询通道:
数屿医械---->产品---->选择目标国家/地区医疗器械数据库--->关键词或条件搜索
查询直达链接:
数据库:数屿医械-医疗器械行业数据服务平台
首页:医疗器械_医疗器械网_中国医疗器械网-数屿医械
②查询范围(数据库):
中国上市医疗器械(54W+)、中国台湾(5W)、香港(近1W)、美国上市前通知510K(近17W)、美国FDA上市前批准、美国医疗器械唯一标识、日本PMDA医疗器械及体外诊断试剂(11W+)、韩国(647W+)等20+个主流国家及地区。数据均来源于各国权威机构官方网站,并做了清洗、印证及整理,以便分析应用。
③查询技巧:
先选择目标国家/地区医疗器械产品数据库。
根据检索框条件进行检索。数屿医械提供两种查询模式,一为精确搜索(包含产品名称、注册/备案人名称、产品备案/注册证号、试用范围/预期用途、结构及组成/主要组成成分)。二为条件筛选(如所属省市区、23类产品目录、批准日期、有效期、注册类型、管理类别、体外诊断试剂/医疗器械、器械状态、国产/进口、医保是/否等。

查询到目标或目标范围医疗器械产品数据后,可进行可视化图表分析及结果导出。或是点击具体产品蓝色字体进行详情页面。详情页面可查询该器械产品所有信息以及历史数据、器械审评数据、唯一标识,还可查询创新/优先医疗器械、医保医用耗材代码、耗材中标、带量采购及抽样调查、召回等全生命周期数据信息。

3.美国:美国药监局FDA(美国医疗器械查询官网)
FDA药监局是美国医疗器械直管机构,也是查询美国境内医疗器械产品生产、上市、销售及使用的权威网站。虽然美国对医疗器械的管理与中国类似,按照危险程度分为三个类别对应管理,即一类伤害最低的采取列名方式(占比47%),二类采取510(k)进行对比(占比46%),三类进行PMA注册(占比7%),但由于语言壁垒,很多人在查询时经常迷失在FDA官网中。下面会对此进行详解。
①查询方法:
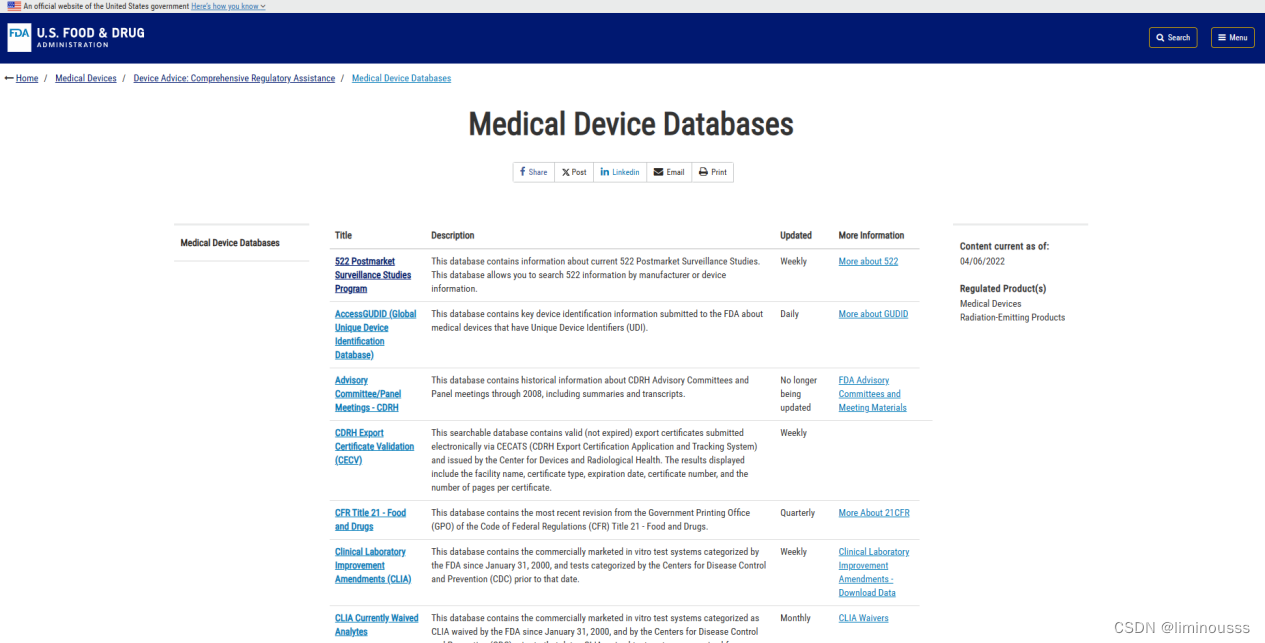
查询通道:
美国药监局FDA---->Medical Devices 医疗设备---->点击All Medical Device Databases ,进入所有医疗器械数据库导航页---->目标医疗器械数据库
所有医疗器械数据库导航页直达链接:https://www.fda.gov/medical-devices/device-advice-comprehensive-regulatory-assistance/medical-device-databases
②查询范围(数据库):
AccessGUDID (Global Unique Device Identification Database):FDA唯一医疗器械产品标识符UDI,全球唯一设备标识数据库
Devices@ FDA:是FDA批准和许可的医疗器械信息目录,企业可以通过产品名称或者公司名字搜索FDA批准或者许可的器械。包含510(k)及PMA数据库。
Premarket Notifications (510(k)s):PMN-510(k)上市前通知,通过510(k)路径申请上市的医疗器械产品均可在此数据库查询。可以按510(k)编号、申请人、设备名称或 FDA 产品代码进行搜索。
Premarket Approvals (PMA):PMA-上市前批准,包含了通过PMA(预先市场批准)途径获得FDA批准的医疗器械信息,可查询器械名称、分类、批准日期等。
De Novo:已批准和已许可的新型中低风险器械产品
4.日本:日本独立行政法人医药品医疗器械综合机构PMDA(日本医疗器械产品查询官网)
日本独立行政法人医药品医疗器械综合机构PMDA是日本医疗器械政府管理机构。其官网提供日文版及英文版两个版本,可在任意一版本中查询到日本所有上市医疗器械产品信息及说明书。
①查询方法(英文版):
查询通道路径:Pharmaceuticals and Medical Devices Agency PMDA--->reviews目录---->informations for approved products in Japan日本国内获批商品信息---->Medical devices 医疗设备---->List of Approved Products 获批产品清单
查询直达链接:https://www.pmda.go.jp/english/review-services/reviews/approved-information/devices/0001.html
②查询说明:
PMDA官网每年均会提供日本国内新的及改进的医疗器械产品清单PDF文件,其官网可查询到2004年4月至2023年6月医疗器械产品信息,尚未建立实时检索的数据库,需进行下载再清洗整理。

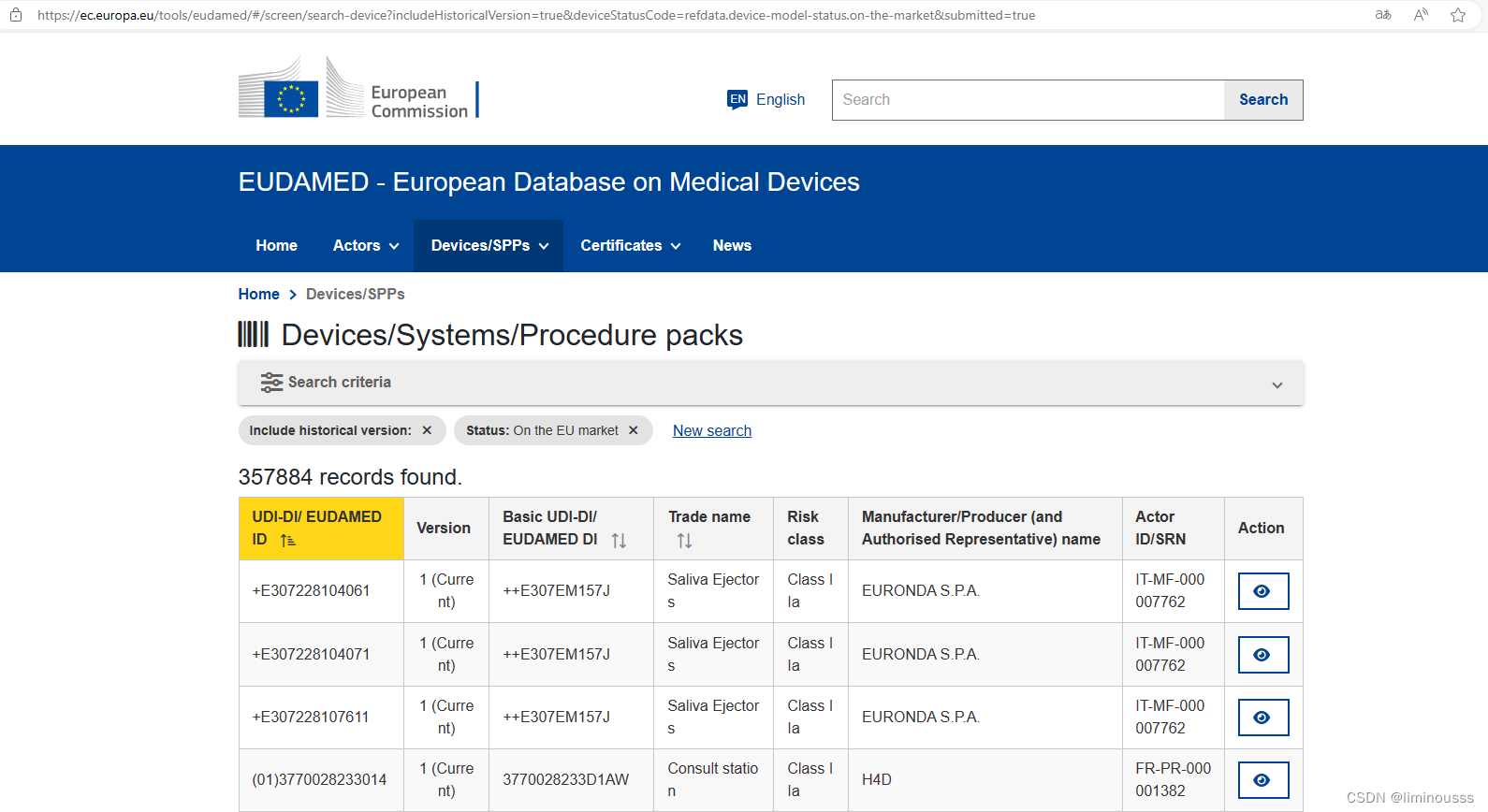
5.欧盟医疗器械数据库EUDAMED
欧盟创建的医疗器械及体外诊断器械法规、企业、UDI和设备注册等数据查询工具,是从欧盟网站(health.ec.europa)独立而成的数据系统,是查询欧盟各成员国已注册上市医疗器械产品的官方平台。
①查询方法
查询通道:
EUDAMED - Die Europäische Kommission欧洲医疗器械数据库---->European Database on Medical Devices首页---->Devices/SPPs---->UDI/Devices registration
查询直达链接:
EUDAMED
②查询范围:
包含欧盟成员国的运营商(生产商、制造商、进口商等)、医疗器械产品唯一设备标识UDI、设备数据、公告机构和证书、临床调查和性能研究、警戒和市场监督信息。
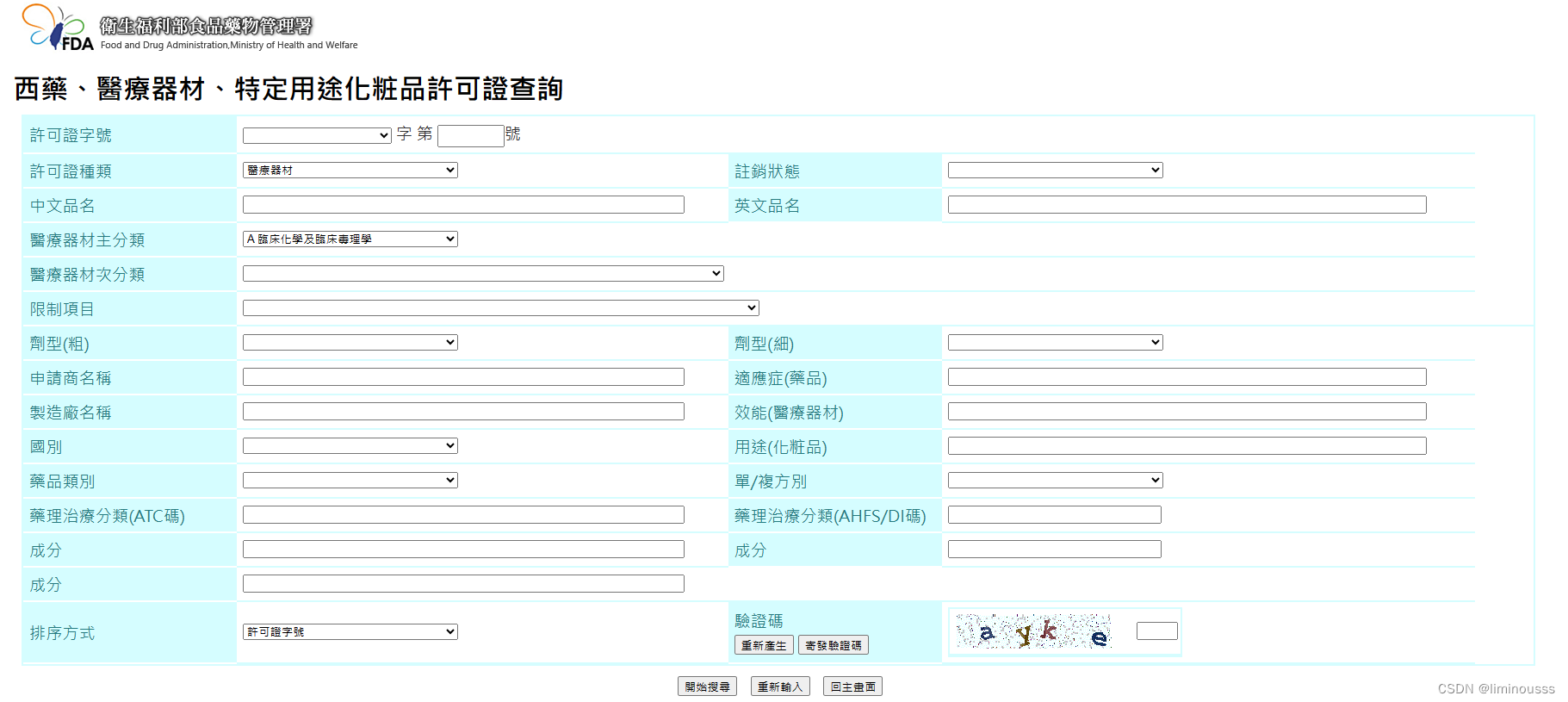
6.中国台湾:中国卫生福利部食品药物管理署 (TFDA)
中国卫生福利部食品药物管理署 (TFDA)是辖区内医疗器械的安全和质量控制、医疗器械监管、临床诊断以及体外诊断的负责机构。
查询通道:卫生福利部食品药物管理署 (TFDA)---->医疗器材---->医疗器材许可证数据库
查询直达链接:https://info.fda.gov.tw/MLMS/H0001.aspx
查询说明:台湾西药、医疗器材及化妆品汇集为统一数据库,可通过许可证或申请商、制造商等相关关键词进行已上市医疗器械的许可证查询。但网站连接不稳定。
7.英国上市医疗器械MHRA
英国医疗器械监管部门MHRA,可查询英国医疗器械与体外诊断试剂的产品管理类别与名称,及相关生产企业与负责人的基本信息。英国上市医疗器械MHRA可在其开设的公共访问注册数据库(PARD)中查询。
查询通道:MHRA站点较多,网站内容复杂,暂不陈述查询通道
查询直达连接:https://pard.mhra.gov.uk/
查询范围:
可查询英国医疗器械评定为合格或已过期的上市医疗器械产品,可通过制造商名称、MHRA参考编号、GMDN®代码、医疗器械类型、医疗器械风险等具体关键词进行精确检索。

8.法国上市医疗器械
法国国家药品安全局ANSM,收录了在法国境内合法上市销售的医疗器械产品信息,这些医疗器械都已经获得了ANSM颁发的上市许可证CE证书。
查询链接直达:
Dispositifs médicaux - ANSM : Agence nationale de sécurité du médicament et des produits de santé

9.加拿大上市医疗器械
加拿大卫生部,收录加拿大已上市医疗器械产品有效许可证数据。加拿大卫生部MDALL在线查询是用于搜索医疗器械产品的HTML应用程序。可以通过公司名称、公司 ID、许可证名称、许可证编号、设备名称、设备标识符进行搜索。
查询链接直达:
Medical devices active licences search (canada.ca)

10.沙特上市医疗器械
沙特阿拉伯(SFDA),收录了在沙特获批准上市销售的较低风险医疗器械产品信息及所有上市医疗器械产品数据。
查询链接直达:
Medical Equipment List | Saudi Food and Drug Authority

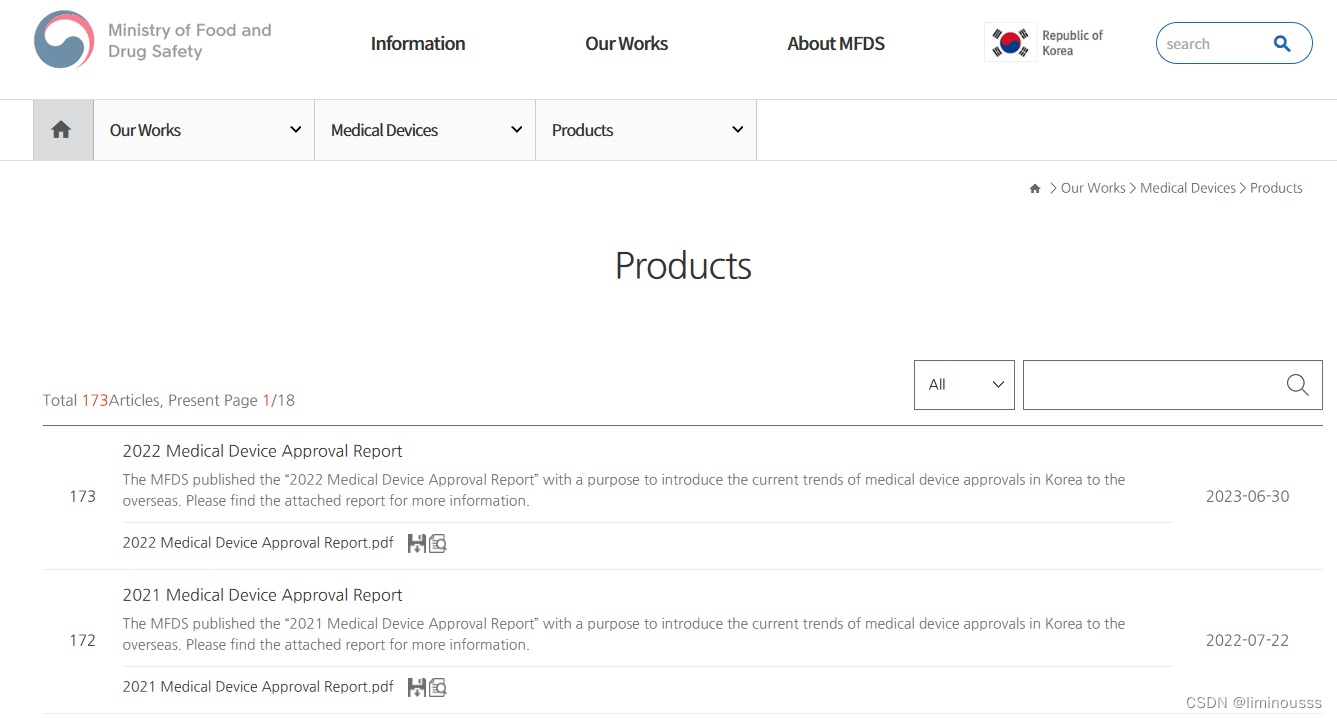
11.韩国上市医疗器械
韩国食品医药品安全管理局(Ministry of Food and Drug Safety,MFDS),收录了所有已经获得MFDS监管许可,可在韩国合法销售的医疗器械信息。
查询链接直达:
Ministry of Food and Drug Safety>Our Works>Medical Devices>Products | Ministry of Food and Drug Safety
12.印度上市医疗器械
印度药品管理局(CDSCO)的医疗器械注册信息,可查询有关印度上市医疗器械的相关监管机构和适应症等信息。
查询链接直达:
https://cdsco.gov.in/opencms/opencms/en/Medical-Device-Diagnostics/Medical-Device-Diagnostics/
13.澳大利亚上市医疗器械
澳大利亚治疗用品管理局TGA是澳大利亚的政府机构,负责评估、评估和监控被定义为治疗用品的产品,对药品、医疗器械和生物制品进行监管。其网站支持查询医疗器械注册信息。
查询链接直达:
https://www.tga.gov.au/resources/artg
14.新加坡上市医疗器械
新加坡卫生科学局(HSA),包含较低风险的A类医疗器械和SMDR数据,可查询新加坡医疗器械产品的基本信息,如产品名称、注册证号、预期用途、产品风险分类、不良事件、变更通知等。
查询链接直达:
HSA | Medical devices
15.俄罗斯上市医疗器械
俄罗斯联邦食品药品监督管理局(Rospotrebnadzor),收录了在俄罗斯获得监管部门批准,可合法生产销售的医疗器械信息。
查询链接直达:
https://rospotrebnadzor.ru/en/
16.意大利上市医疗器械
意大利药物管理局AIFA,展示意大利医疗器械产品的分类注册状态以及生产企业,并且提供需遵守的相关CE法规以及CE分类等详细信息。
查询链接直达:
https://www.aifa.gov.it/en/home
17.巴西上市医疗器械
巴西医疗器械监管部门ANVISA,提供有关巴西医疗器械产品管理类别与风险等级描述,注册证编号以及注册证状态等详细信息,全部器械注册证详细信息与部分产品说明书提供全文查询、下载。
查询链接直达:
https://www.gov.br/anvisa/pt-br/english/regulation-of-products/medical-devices
18.以色列上市医疗器械
以色列卫生部,提供有关以色列医疗器械的产品名称与注册证编号,也可查询相关生产企业与制造国的基本信息。
查询链接直达:
https://israeldrugs.health.gov.il/#!/byDrug
19.秘鲁上市医疗器械
在秘鲁,负责医疗器械监管的机构是 Dirección General de Medicamentos,Insumos y Drogas(DIGEMID)。该机构隶属于卫生部(Ministerio de Salud或MINSA)。秘鲁医疗器械主管机构Digemid提供各类已上市医疗器械产品查询。
查询链接直达:
Dispositivos Médicos – DIGEMID
20.阿根廷上市医疗器械
阿根廷国家食品药品及医疗技术管理局ANMAT,包含了产品的基本信息,如产品名称、生产商名称、注册证号、产品规格型号等,支持公开数据文件下载。
查询链接直达:
helena.anmat.gob.ar/Boletin/
21.葡萄牙上市医疗器械
葡萄牙国家药品和医疗产品管理局(INFARMED),收录了在葡萄牙获得上市许可的医疗器械信息。
查询链接直达:
Pesquisa Dispositivos Médicos - INFARMED, I.P.
22.马来西亚上市医疗器械
马来西亚医疗器械管理监督局(MDA),收录了马来西亚批准上市的医疗器械产品信息,这些医疗器械都已经通过MDA的严格审批流程。可输入提交编号、注册编号、机构名称或品牌名称,然后按搜索按钮。对于未出现在搜索结果中的那些数据,搜索的设备为“未注册”或“已过期”或“已暂停”或“已取消”。
查询链接直达:
Public Search - Malaysia Medical Device Register (MMDR)

23.罗马尼亚:罗马尼亚国家药品和医疗器械局 (ANMDMR)
罗马尼亚国家药品和医疗器械局 (ANMDMR) 隶属于卫生部,是人用药品、医疗器械以及人用药品、高性能医疗器械和设备的医疗技术评估领域的国家主管机构,位于罗马尼亚的制造商或制造商的授权代表有义务在ANMDMR注册,并可进行公开查询。
查询链接直达:
F1, F2 - Producătorii cu sediul în România care introduc dispozitive medicale pe piață sub propriul nume și reprezentanții autorizați în UE care introduc pe piața din România dispozitive medicale fabricate de producatori cu sediul social care nu se află pe teritoriul UE * - ANMDMR Nomenclatorul Dispozitivelor Medicale