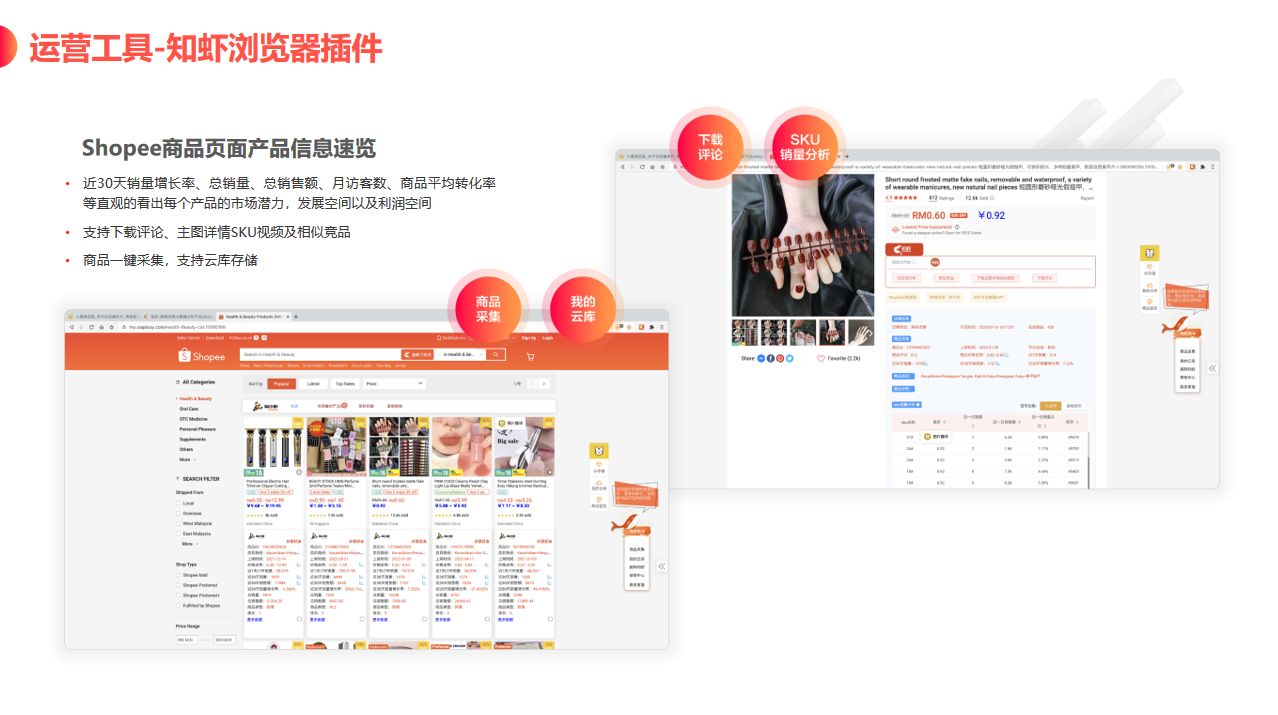
2015年以前,参比制剂对于仿制药的研究无关紧要,但推出了’仿制药一致性评价’后,参比制剂的选择成为了决定仿制药成功与否的关键因素,如今在进行仿制药研究时,首要任务就是确定仿制目标,也就是参比制剂。
而参比制剂选择的主要参考依据是通过查看各国建立的详细参比制剂目录,如我国主要使用的美国FDA参比制剂目录、WHO 世界卫生组织参比制剂目录、日本(PMDA)参比制剂目录、中国官方的NMPA参比制剂目录,其中日本的参比制剂目录中增加了多条特征溶 出曲线测定法、测定结果与图示,使得更具参照性,而我国的参比制剂目录,更多的是圈出了参比制剂的选择范围。
所以精通这几个参比制剂目录的查看方法是仿制药研发员的基本功,还不知道如何查的或是已经忘了如何查的,请好好收藏本文,本文将以保姆式的教学步骤详细讲解美国FDA、日本PMDA、中国NMPA、世卫WHO以及高效的参比制剂目录查询方法。
①日本PMDA官网查询
因为日本内容更具参照性,所以讲解的更加细致一些。
日本药品的参比制剂目录存于两个地方,固体口服制剂通过日本橙皮书查找,其他制剂如注射剂可以通过PMDA数据库或药融云数据库进行查找
Ⅰ、日本橙皮书(www.jp-orangebook.gr.jp)
进入网址-->选择’品质再评价...技术情报’-->选择’品目情报’or’品目情报检索’-->展示页面即日本仿制药参比制剂目录(固体口服)

步骤(一)

步骤二

日本橙皮书-参比制剂目录(检索)
Ⅱ、PMDA数据库(www.pmda.go.jp)
进入网址-->选择(处方药or非处方药)-->搜索药品(活性成分、商品名、企业名称、组成成分)-->申请资料概要-->同种同效果药品一览(一般参比制剂为该目录第一个)

步骤1
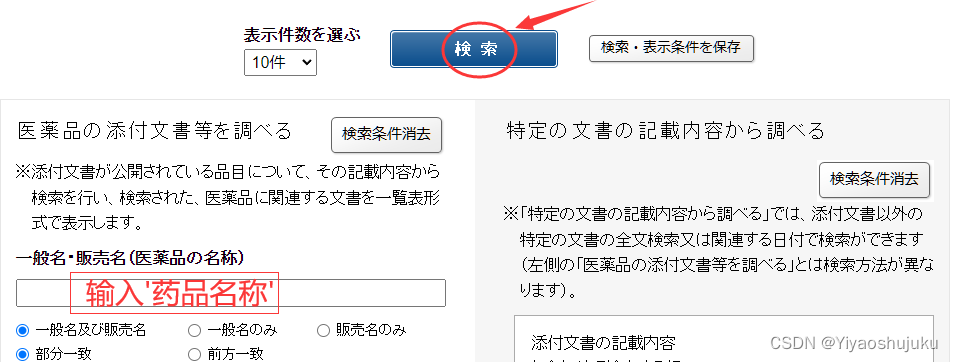
步骤二

步骤三

步骤四
②NMPA&CDE官网查询
NMPA官网(www.nmpa.gov.cn)
官网的仿制药参比制剂目录主要通过文件公告的形式发布,如最新发布的第七十三批仿制药参比制剂目录,可以直接进入官网主页搜索框搜索’参比制剂目录第七十三批’

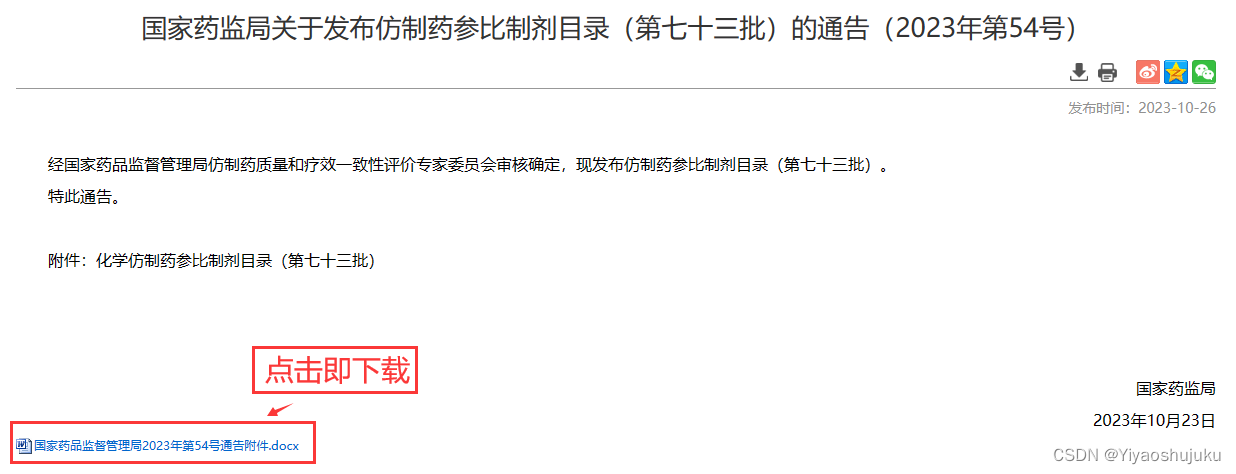
CDE官网查询(www.cde.org.cn)
CDE网站查询与NMPA一样进入网站首页搜索’仿制药参比制剂目录’,可以看到与NMPA不一样的是CDE为各批次目录的征求意见稿
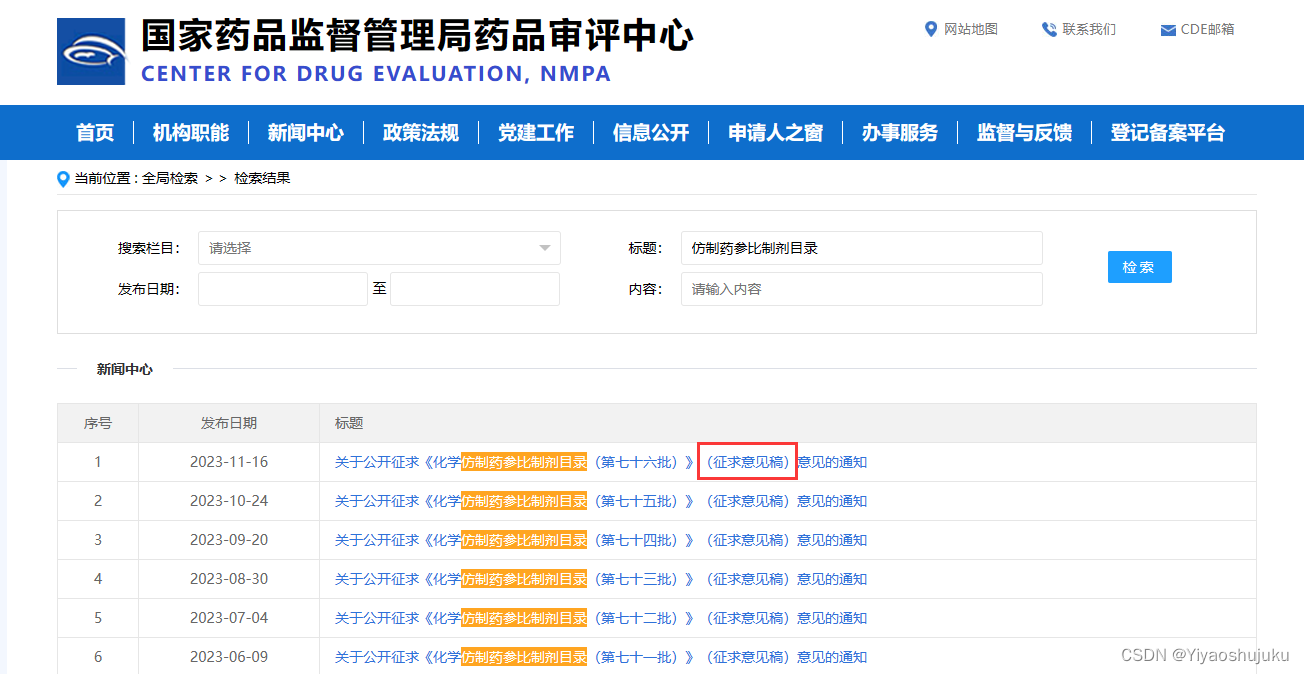
③药融云-医药数据库系统查询(www.pharnexcloud.com)
药融云-仿制药参比制剂目录数据库(免费查阅)-收载了13000余条数据,包括了国家正式目录、国家公示目录、征求意见稿、增补品种目录和未通过审议品种目录,数据来源于cde官方网站和NMPA官方网站公告。
为了方便选择仿制药参比制剂提供参考,同时还提供美国橙皮书、日本橙皮书、无推荐参比制剂药品目录、参比制剂备案、WHO参比制剂目录、一致性评价等数据库,可以很方便的查看主要国家关于仿制药各类文件信息。
进入网址-->选择’个人版’或’企业版’-->选择’一致性评价’-->选择目标参比制剂目录数据库-->点击下载目标文件

(药融云-个人版)
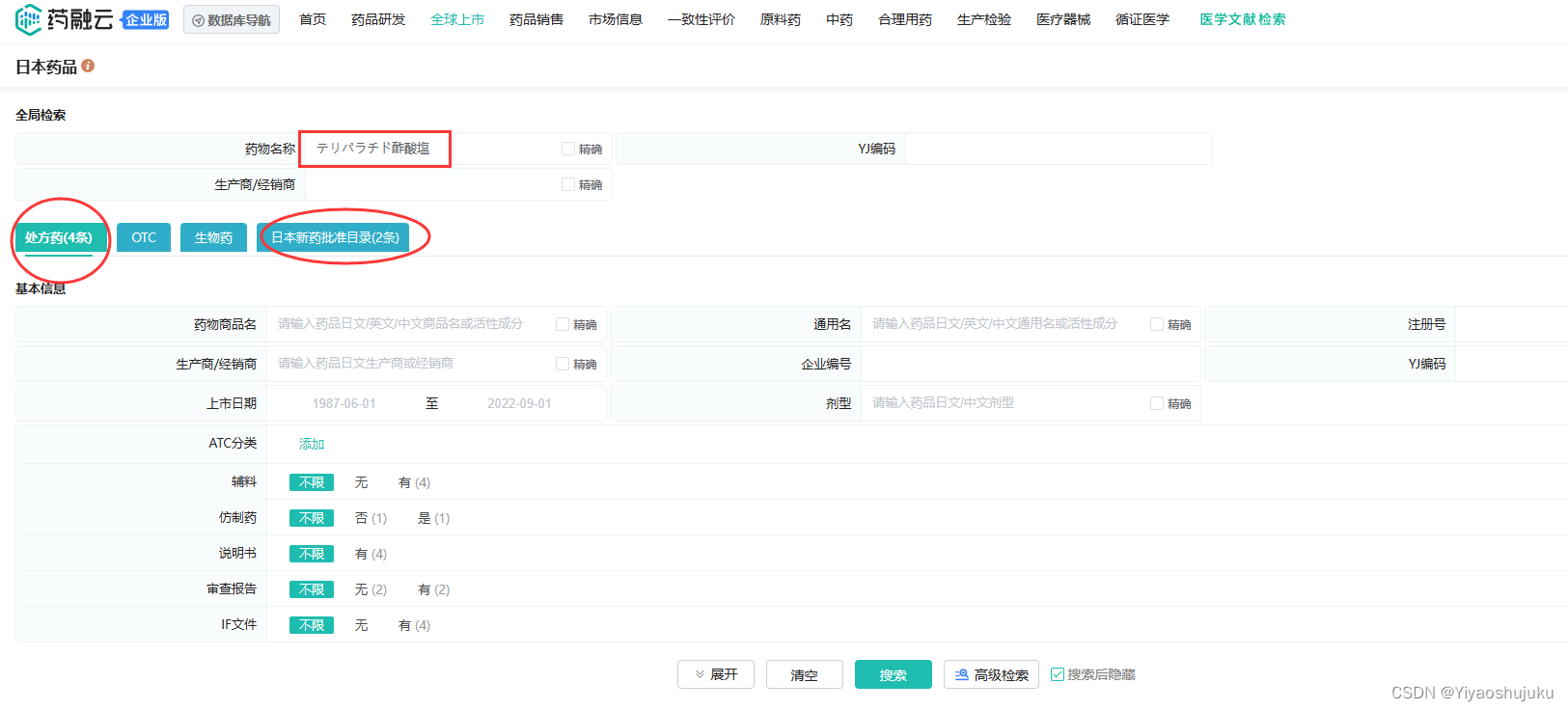
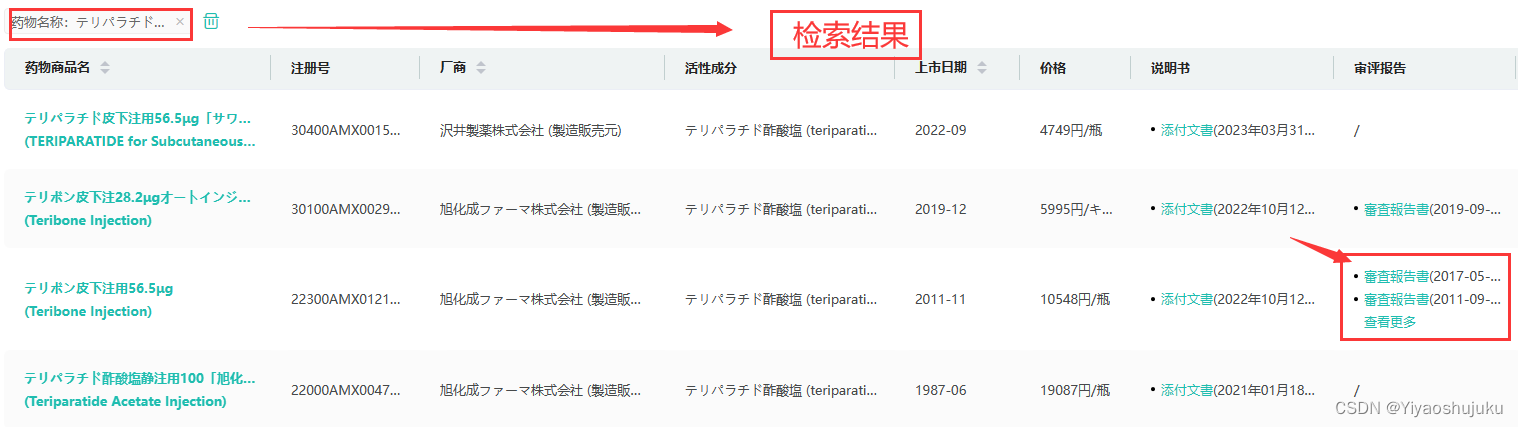
(企业版全球上市-日本药品)
④美国FDA官网查询
Drugs@FDA数据库(www.accessdata.fda.gov/scripts/cder/daf/index.cfm)
在fda中可以直接通过Drugs@FDA数据库查看仿制药参比制剂信息,进入网址

在搜索框输入活性成分Dapagliflozin,进入下图界面:
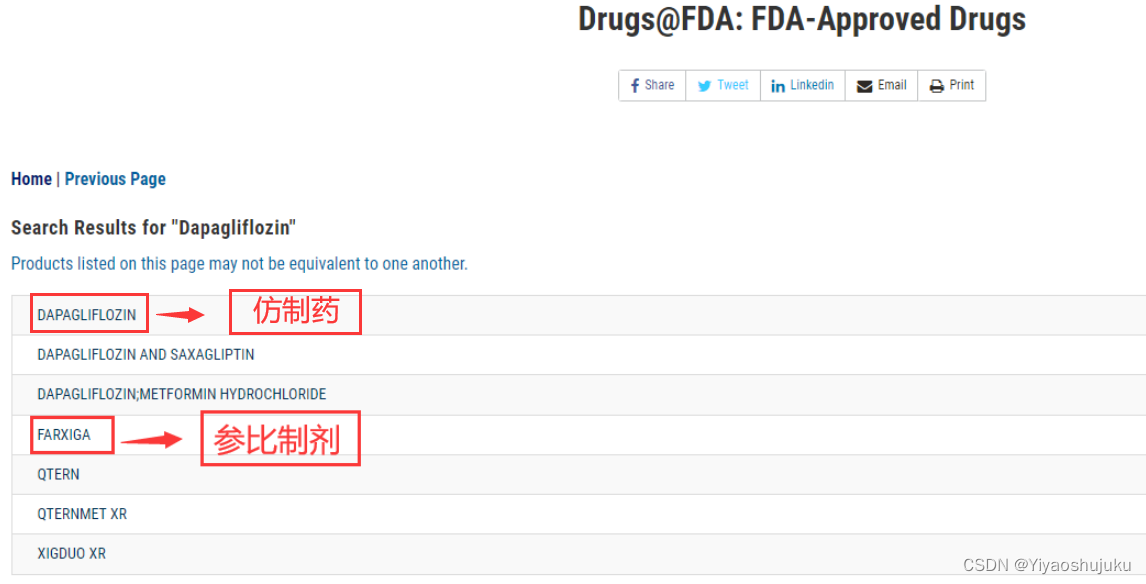
可查询到仿制药及参比制剂信息,点击进入参比制剂,可看到审评报告及说明书等信息
根据以上几种参比制剂目录信息的查询方法可以快速查阅参比制剂相关信息,为选择仿制药参比制剂提供参考信息,提高企业选择参比制剂效率,增加首个获得评价同类药品认可的几率。帮助医药人员做出准确的药物选择和决策。